题目内容
4.已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O.上述反应中,氧化剂与还原剂的物质的量之比为2:3.分析 3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O中,Cu元素的化合价由0升高为+2价,N元素的化合价由+5价降低为+2价,以此来解答.
解答 解:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O中,Cu元素的化合价由0升高为+2价,N元素的化合价由+5价降低为+2价,Cu为还原剂,HNO3为氧化剂,3molCu失去电子与2molN得到电子相同,则氧化剂与还原剂的物质的量之比为2:3,
故答案为:2:3.
点评 本题考查氧化还原反应,题目难度不大,把握反应中元素的化合价变化为解答的关键,.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
19.如图表示298K时N2与H2反应过程中的能量变化.根据如图叙述正确的是( )
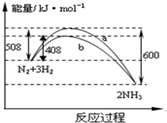

| A. | 该反应的热化学方程式为$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)?NH3(g)△H=-92kJ•mol-1 | |
| B. | 不用催化剂,生成1molNH3放出的热量为46kJ,加入催化剂,生成1molNH3放出的热量为小于46kJ | |
| C. | 加入催化剂,降低了正反应的活化能,升高了逆反应的活化能 | |
| D. | 在温度、体积一定的条件下,通入1molN2和3molH2,反应后放出的热量为Q1,若通入2molN2和6molH2,反应后放出的热量为Q2,则Q1<0.5Q2<92KJ |
16.MgO可用于制备特种陶瓷,在一定条件下,通过下列反应制备,MgSO4(s)+CO(g)═MgO(s)+CO2(g)+SO2(g)△H>0.上述反应达到平衡后保持其他条件不变,下列说法正确的是( )
| A. | 该反应在高温下不容易自发进行 | B. | 升高温度,混合气体的密度增大 | ||
| C. | 压缩容器,反应吸收的热量不变 | D. | 分离出部分MgO,可增大CO的转化率 |
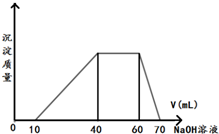 有一澄清透明的溶液,可能有NH4+、Fe3+、H+、Mg2+、Al3+、I-、CO32-等离子,现分别取溶液进行下列实验:
有一澄清透明的溶液,可能有NH4+、Fe3+、H+、Mg2+、Al3+、I-、CO32-等离子,现分别取溶液进行下列实验: