题目内容
2.25℃时,硫氢化钾(KHS)溶液里存在下列平衡:(a)HS-+H2O?OH-+H2S
(b)HS-?H++S2-
(1)b(填序号,下同)是电离平衡;a是水解平衡.
(2)若向其中加入硫酸铜溶液时,可生成CuS沉淀,则电离平衡向正向(填“正向”或“逆向”)移动;水解平衡向逆向(填“正向”或“逆向”)移动;.
(3)若将溶液加热至沸腾,c(OH-)•c(H+)将变大(填“大”或“小”).
(4)若在0.1mol•L-1硫酸铜溶液中加入适量NaHS固体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是0.2mol•L-1.
分析 (1)根据电离和水解的定义来分析解答;
(2)当向其中加入硫酸铜溶液时,生成了CuS沉淀,促进HS-的电离,HS-浓度减小,水解程度减小,溶液中H+的浓度增大;
(3)水的电离是吸热反应,升高温度促进其电离;
(4)根据溶液的电中性计算H+浓度.
解答 解:(1)根据电离和水解定义知,b是电离平衡,a是水解平衡,故选:b;a;
(2)向其中加入硫酸铜溶液时,生成了CuS沉淀,S2-浓度减小,促进HS-的电离,电离平衡向右移动,溶液中H+的浓度增大,HS-浓度减小,水解平衡向左移动,水解程度减小,
故答案为:正向;逆向;
(3)水的电离是吸热反应,升高温度促进水电离,所以水的离子积常数增大,故答案为:大;
(4)在0.1mol•L-1硫酸铜溶液中加入适量NaHS固体,使Cu2+完全沉淀为CuS,此时溶液中的溶质为硫酸,c(SO42-)不变,为0.1mol•L-1,由电荷守恒可知c(H+)为0.2mol•L-1,
故答案为:0.2.
点评 本题考查了弱电解质的电离及其盐类水解,明确弱电解质电离及水解特点是解本题关键,注意浓度对平衡移动的影响,难度不大.

练习册系列答案
相关题目
13.下列图示与对应的叙述不相符的是( )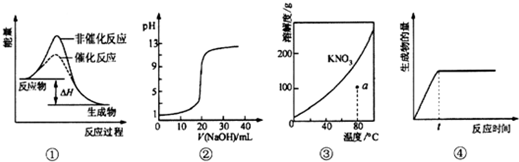

| A. | ①表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| B. | ②表示0.1 mo1•L-1NaOH溶液滴定20 mL 0.1 mo1•L-1HCl溶液所得到的滴定曲线 | |
| C. | ③表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 | |
| D. | 某可逆反应生成物的量随反应时间关系如图④所示,在t时反应物转化率达到最大 |
10.分类法在化学学科的发展中起到了非常重要的作用.下列属于有机物的是( )
| A. | H2SO4 | B. | KAl(SO4)2 12H2O | C. | C2H5OH | D. | Ca(OH)2 |
17.下面关于硅的叙述中,正确的是( )
| A. | 粗硅制备单晶硅不涉及氧化还原反应 | |
| B. | 硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位 | |
| C. | 硅的化学性质不活泼,在自然界中可以以游离态存在 | |
| D. | 硅在电子工业中,是重要的半导体材料 |
7.下列叙述正确的是( )
| A. | 95℃纯水的pH<7,说明加热可导致水呈酸性 | |
| B. | pH=3的醋酸溶液稀释至10倍后pH=4 | |
| C. | 0.2 mol/L的盐酸与0.1 mol/L的盐酸等体积水混合后pH=1.5 | |
| D. | pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH<7 |
3. “低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题
“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:5C+4KMnO4+6H2SO4=5CO2↑+4MnSO4+2K2SO4+6H2O
(2)将不同量的CO(g)和H2O(g)分别通入到体积为 2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如下二组数据:
①实验1中以v(CO2)表示的反应速率为0.13mol/(L•min)(保留二位小数,下同).
②实验2条件下平衡常数K=0.17,该反应为放(填“吸”或“放”)热反应.
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566.0 kJ/mol
③H2O(g)=H2O(l))△H=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ/mol
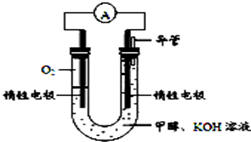
(4)某实验小组依据甲醇燃烧的反应原理,设计如右图所示的电池装置.
①该电池正极的电极反应为O2+H2O+4e-=4OH-.
②该电池工作时,溶液中的OH-向负极移动.
 “低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题
“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:5C+4KMnO4+6H2SO4=5CO2↑+4MnSO4+2K2SO4+6H2O
(2)将不同量的CO(g)和H2O(g)分别通入到体积为 2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如下二组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
②实验2条件下平衡常数K=0.17,该反应为放(填“吸”或“放”)热反应.
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566.0 kJ/mol
③H2O(g)=H2O(l))△H=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ/mol
(4)某实验小组依据甲醇燃烧的反应原理,设计如右图所示的电池装置.
①该电池正极的电极反应为O2+H2O+4e-=4OH-.
②该电池工作时,溶液中的OH-向负极移动.
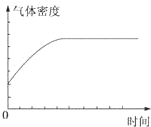
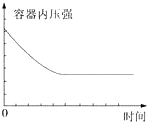
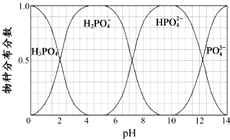 磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH 的关系如图所示.
磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH 的关系如图所示.