题目内容
12.在某恒容密闭容器中进行如下可逆反应:2M(g)+N(g)?W(?)+4Q(g)△H<0,起始投料只有M和N.下列示意图正确且能表示该可逆反应达到平衡状态的是( )| A. | 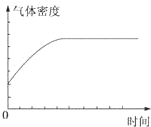 | B. | 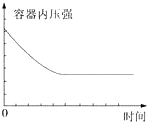 | ||
| C. | 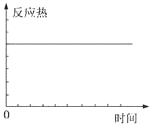 | D. | 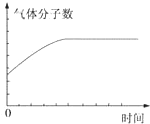 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、如果W是非气态,则密度开始减小,而不是增大;如果W是气体气体密度始终不变,所以不能作平衡状态的标志,故A错误;
B、不论W是何状态,开始容器内的压强是增大,而不是减少,故B错误;
C、反应热始终是一个定值,不能作平衡状态的标志,故C错误;
D、不论W是何状态,反应开始物质的量增加,分子数增多,一旦分子数不变说明达平衡状态,故D正确;
故选D.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
2.NA代表阿伏加德罗常数的值,下列有关说法正确的是( )
| A. | 1 mol 羟基(-OH)含有的电子数为10 NA | |
| B. | 高温下,0.2 mol Fe与足量水蒸气反应,生成H2的分子数为0.3 NA | |
| C. | 7.8 g Na2S、Na2O2的固体混合物中含有的阴离子数为0.1 NA | |
| D. | 用惰性电极电解饱和食盐水,电路中通过NA个电子,则阳极产生气体11.2 L |
3.下列反应的离子方程式书写正确的是( )
| A. | 硫酸铜溶液与氢氧化钡溶液混合:Ba2++SO42-═BaSO4↓ | |
| B. | 大理石投入稀硝酸中:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 氨水与硫酸铝溶液混合:Al3++4NH3?H2O═AlO2-+4NH4++2H2O | |
| D. | 氯水通入水中:Cl2+H2O═Cl-+ClO-+2H+ |
20.甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如下图所示(部分产物已略去),如表各组物质中不能按图示关系转化的是( )
| 选项 | 物质转化关系 | 甲 | 乙 | 丙 | 丁 |
| A | 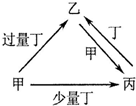 | NaOH | NaHCO3 | Na2CO3 | CO2 |
| B | C | CO | CO2 | O2 | |
| C | Fe | Fe(NO3)3 | Fe(NO3)2 | HNO3 | |
| D | AlCl3 | NaAlO2 | Al(OH)3 | NaOH |
| A. | A | B. | B | C. | C | D. | D |
7.常温下,0.1mol/L的下列溶液中,水的电离程度大小排列顺序正确的是( )
①AlCl3
②KNO3
③NaOH
④NH3•H2O.
①AlCl3
②KNO3
③NaOH
④NH3•H2O.
| A. | ①>②>③>④ | B. | ①>②>④>③ | C. | ③>④>②>① | D. | ①=②=③=④ |
17.按要求回答下列问题:
(1)实验室常用NaOH溶液来进行洗气和提纯,当100mL3mol/L的NaOH溶液吸收标准状况下4.48LCO2时,所得溶液中各离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
(2)常温下向一定体积的0.1mol/L醋酸溶液中加水稀释后,下列说法正确的是CD.
A.溶液中导电粒子的数目减小
B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$不变
D.溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(O{H}^{-})}$减小
(3)①常温下将0.15mol/L稀硫酸V1mL与0.1mol/LNaOH溶液V2mL混合,所得溶液的pH为1,则V1:V2=1:1(溶液体积变化忽略不计).
②常温下若溶液由pH=3的HA溶液V1mL与pH=11的NaOH溶液V2mL混合而得,则下列说法正确的是AD
A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7 mol/L
B.若V1=V2,反应后溶液pH一定等于7
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈碱性,则V1一定小于V2
(4)常温下,浓度均为0.1mol/L的下列五种溶液的pH值如表所示:
①根据表中数据,将浓度均为0.01mol/L的下列四种酸的溶液分别稀释100倍,pH变化最小的是A.
A.HCN B.HClO C.Na2CO3 D.CH3COOH
②根据以上数据,判断下列反应可以成立的是AB.
A.CH3COOH+Na2CO3═NaHCO3+CH3COONa
B.CH3COOH+NaCN═CH3COONa+HCN
C.CO2+H2O+2NaClO═Na2CO3+2HClO
D.NaHCO3+HCN═NaCN+CO2+H2O
(5)几种离子开始沉淀时的pH如下表:
当向含相同浓度Cu2+、Mg2+、Fe2+离子的溶液中滴加NaOH溶液时,Cu2+(填离子符号)先沉淀,Ksp[Fe(OH)2]<Ksp[Mg(OH)2](填“>”、“=”或“<”)
(1)实验室常用NaOH溶液来进行洗气和提纯,当100mL3mol/L的NaOH溶液吸收标准状况下4.48LCO2时,所得溶液中各离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
(2)常温下向一定体积的0.1mol/L醋酸溶液中加水稀释后,下列说法正确的是CD.
A.溶液中导电粒子的数目减小
B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$不变
D.溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(O{H}^{-})}$减小
(3)①常温下将0.15mol/L稀硫酸V1mL与0.1mol/LNaOH溶液V2mL混合,所得溶液的pH为1,则V1:V2=1:1(溶液体积变化忽略不计).
②常温下若溶液由pH=3的HA溶液V1mL与pH=11的NaOH溶液V2mL混合而得,则下列说法正确的是AD
A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7 mol/L
B.若V1=V2,反应后溶液pH一定等于7
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈碱性,则V1一定小于V2
(4)常温下,浓度均为0.1mol/L的下列五种溶液的pH值如表所示:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
A.HCN B.HClO C.Na2CO3 D.CH3COOH
②根据以上数据,判断下列反应可以成立的是AB.
A.CH3COOH+Na2CO3═NaHCO3+CH3COONa
B.CH3COOH+NaCN═CH3COONa+HCN
C.CO2+H2O+2NaClO═Na2CO3+2HClO
D.NaHCO3+HCN═NaCN+CO2+H2O
(5)几种离子开始沉淀时的pH如下表:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
4.二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理如下:2NaClO3+4HCl═2ClO2↑+Cl2↑+2H2O+2NaCl,下列关于该反应的说法正确的是( )
| A. | 浓盐酸在反应中仅体现还原性 | |
| B. | 被氧化和被还原的物质的物质的量之比为1:1 | |
| C. | 每生成0.1molClO2转移0.2mol电子 | |
| D. | 氧化性:NaClO3<Cl2 |
1.下列说法中不正确的是( )
| A. | 含SO2的烟气可用石灰乳吸收后再排放,以减少对空气污染 | |
| B. | 汽车尾气、工业排放、建筑扬尘、垃圾焚烧等都是造成雾霾天气的主要原因 | |
| C. | 绿色化学的核心是对环境产生的污染进行治理 | |
| D. | PM2.5由于颗粒小,在空气中存在时间长,对人体健康危害大 |