题目内容
10.海洋植物如海带中含有丰富的碘元素,碘元素以碘离子的形式存在.某研究性学习小组设计如下实验从海带中提取碘,请你完成下面相关问题:海带$\stackrel{①}{→}$海带灰$\stackrel{②浸泡}{→}$海带灰悬浊液$\stackrel{③}{→}$含I-的溶液$→_{H_{2}O_{2}}^{④稀硫酸}$含I2的水溶液$\stackrel{⑤}{→}$含I2有机溶液$\stackrel{⑥}{→}$晶体碘.
(1)步骤①的名称为灼烧,需要用到的仪器有坩埚、酒精灯、泥三角.
(2)步骤④的离子反应为2I-+H2O2+2H+=I2+2H2O.
(3)步骤⑤的名称为萃取分液,可供选择的试剂是B(填编号).
A.酒精 B.四氯化碳 C.乙酸 D.蔗糖溶液.
(4)怎样检验步骤④后得到的溶液中含有碘单质加入淀粉试液,若变蓝色,说明有碘单质,反之没有.
(5)步骤⑤的名称为萃取,最后晶体碘在蒸馏烧瓶(填仪器名称)里聚集.
分析 实验室从海带中提取碘:海带灼烧成灰①,浸泡溶解得到海带灰悬浊液②,通过过滤③,得到不溶的残渣,滤液为含碘离子的溶液,加入酸和氧化剂H2O2④,将碘离子氧化成碘单质,利用有机溶剂苯萃取出碘单质⑤,再通过蒸馏提取出碘单质⑥.
(1)根据实验操作步骤①灼烧来分析用到的实验仪器;
(2)过氧化氢在酸溶液中氧化碘离子为单质碘;
(3)同一溶质在不同溶剂中的溶解度不同的溶质可以采用萃取的方法分离;根据萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多分析;
(4)淀粉遇碘变蓝,利用淀粉检验碘单质;
(5)利用有机溶剂苯萃取出碘单质,碘易升华,碘晶体聚集在烧瓶中.
解答 解:实验室从海带中提取碘:海带灼烧成灰,浸泡溶解得到海带灰悬浊液,通过过滤,得到不溶的残渣,滤液为含碘离子的溶液,加入氧化剂,将碘离子氧化成碘单质,H2O2+2I-+2H+=I2+2H2O,利用有机溶剂萃取出碘单质,再通过蒸馏提取出碘单质.
(1)步骤①是固体灼烧,灼烧固体物质一般使用(瓷)坩埚,而坩埚加热需要用泥三脚支撑然后放在三脚架上,三脚架下面的空间放酒精灯.
故答案为:灼烧;坩埚、酒精灯、泥三角;
(2)将含碘离子溶液中加入氧化剂是为了将碘离子氧化,过氧化氢在酸溶液中氧化成单质碘,离子方程式为2I-+H2O2+2H+=I2+2H2O,
故答案为:2I-+H2O2+2H+=I2+2H2O;
(3)操作⑤是将碘水转化为含碘的有机溶液,需用对卤素单质溶解能力强的有机溶剂把碘从碘水中提取出来,对应进行的实验操作是萃取,利用碘易溶于有机溶剂的性质来进行提取,利用碘易溶于有机溶剂的性质来进行提取,须注意:选择的能提取碘的试剂除了对I2有强的溶解能力处,还必须难溶于水,否则不能进行分液分离,符合条件的是四氯化碳,酒精、乙酸、蔗糖都易溶于水,不能分层,
故答案为:萃取分液;B;
(4)碘遇淀粉试液变蓝色,所以可以用淀粉试液检验是否含有碘,其检验方法为:向该溶液中滴加淀粉试液,如果溶液变蓝色,则证明含有碘,否则不含碘,
故答案为:加入淀粉试液,若变蓝色,说明有碘单质,反之没有;
(5)将碘离子氧化成碘单质,利用有机溶剂苯萃取出碘单质⑤,所以步骤⑤的名称为萃取,碘易升华,有机溶剂沸点较低蒸发,所以碘晶体聚集在烧瓶中,
故答案为:萃取;蒸馏烧瓶.
点评 本题以海水资源及其综合利用为载体考查了物质的分离和提纯,明确实验原理是解本题关键,涉及萃取剂的选取、基本操作方法的选取、仪器的选取等知识点,根据萃取剂的选取标准、物质的性质等知识点来分析解答即可,题目难度不大.

| A. | (CH3)3COH的名称:1,1-二甲基乙醇 | B. | 有机物CH3CH=CHCH2OH的键线式为: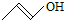 | ||
| C. | 乙醇分子的球棍模型: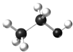 | D. | 氨基的电子式: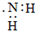 |
| A. | 氯化氢分子的电子式: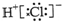 | B. | 乙烯的分子式:C2H6 | ||
| C. | 二氧化碳分子的结构式:O-C-O | D. | CH4分子的球棍模型: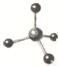 |
(1)该废氨水中氨的物质的量浓度为9×10-3mol/L.
(2)对废氨水进行加热蒸发得到NH3,使废氨水中的NH3的浓度降为17mg•L-1.忽略蒸发前后废氨水体积变化,则上述体积的废氨水蒸发出来的NH3的物质的量为4800 mol.(以下计算结果均保留两位小数)
(3)蒸发得到的NH3可用于制备NO.4NH3+5O2→4NO+6H2O;(不考虑NO与氧气的反应),设空气中氧气的体积分数为0.20,氮气体积分数为0.80.
①为使NH3恰好完全氧化为NO,氨-空气混合物中氨的体积分数为0.14.
②氨催化氧化制取NO同时会发生副反应:4NH3+3O2→2N2+6H2O.将1L NH3混合10L空气后通入反应器,反应完成后,测得混合气体中不含NH3,而O2和N2的物质的量之比为1:10,试求参加主反应的氨占原料氨的体积百分含量.
(4)废氨水可用于脱除烟气中的SO2.氨水吸收烟气中SO2经氧化后生成(NH4)2SO4和NH4HSO4混合物.现称取不同质量的混合物进行实验,结果如下:
| NaOH 溶液体积/mL | 40.00 | 40.00 | 40.00 |
| 样品质量/g | 7.75 | 15.50 | 23.25 |
| 氨气质量/g | 1.87 | 1.87 | 1.7 |
| A. | 以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,故溶液pH不变 | |
| B. | 电解稀氢氧化钠溶液要消耗OH-,故溶液pH减小 | |
| C. | 电解硫酸钠溶液,在阴极上发生反应:4OH--4e-═2H2O+O2↑ | |
| D. | 电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:1 |
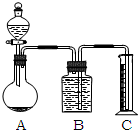 甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验.
甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验.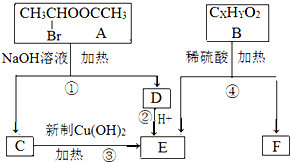 六种有机物之间的转化关系如图.已知:一个碳原子上连有两个羟基的结构极不稳定,易发生变化:R-CH(OH)2→RCHO+H2O
六种有机物之间的转化关系如图.已知:一个碳原子上连有两个羟基的结构极不稳定,易发生变化:R-CH(OH)2→RCHO+H2O
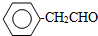 或
或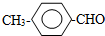 或(邻位、间位).
或(邻位、间位).