题目内容
把锌粒放入盛有稀盐酸的容器中,产生H2的速率与下列因素无关的是( )
| A、盐酸的体积 |
| B、溶液的温度 |
| C、锌粒的大小 |
| D、盐酸的浓度 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:锌粒投入盛有稀盐酸反应的实质是Zn+2H+=Zn++H2↑,影响反应速率的外界因素有浓度、温度、固体表面积、催化剂等因素,以此解答.
解答:
解:A.盐酸的体积大小与反应速率无关,故A选;
B.升高温度,反应速率增大,故B不选;
C.锌粒的表面积大小不同,反应速率不同,故C不选;
D.增大盐酸的浓度,H+浓度增大,反应速率增大,故D不选.
故选A.
B.升高温度,反应速率增大,故B不选;
C.锌粒的表面积大小不同,反应速率不同,故C不选;
D.增大盐酸的浓度,H+浓度增大,反应速率增大,故D不选.
故选A.
点评:本题考查反应速率的影响因素,为高频考点,侧重于学生的分析能力的考查,题目难度中等,注意把握影响反应速率的因素.

练习册系列答案
相关题目
下列有关说法正确的是( )
①如果某化合物只含共价键,则其一定是共价化合物
②有阴离子存在的物质中一定存在阳离子
③碳、氮形成的氢化物常温下都是气态
④非金属单质在反应中都只能作氧化剂,具有强氧化性
⑤金属氧化物不一定是碱性氧化物
⑥稀有气体不活泼是因为它们原子最外层都达到8e-稳定结构.
①如果某化合物只含共价键,则其一定是共价化合物
②有阴离子存在的物质中一定存在阳离子
③碳、氮形成的氢化物常温下都是气态
④非金属单质在反应中都只能作氧化剂,具有强氧化性
⑤金属氧化物不一定是碱性氧化物
⑥稀有气体不活泼是因为它们原子最外层都达到8e-稳定结构.
| A、①②⑤ | B、②③④ |
| C、①②⑥ | D、②③⑤ |
市场上经常见到的标记为Li-ion的电池.它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料.这种锂离子电池的电池反应式为:Li+2Li0.35NiO2
2Li0.85NiO2,下列说法不正确的是( )
| 放点 |
| 充电 |
| A、放电时,负极的电极反应式:Li-e-=Li+ |
| B、充电时,Li0.85NiO2既发生氧化反应又发生还原反应 |
| C、该电池既能用酸溶液又能用碱溶液作电解质溶液 |
| D、放电过程中Li+向正极移动 |
下列反应属于放热反应的是( )
| A、氢氧化钡晶体和氯化铵晶体的反应 |
B、 能量变化如图所示的反应 |
| C、化学键断裂吸收的总热量比化学键生成放出的总热量多的反应 |
| D、镁与盐酸的反应 |
下列装置能够组成原电池并发生原电池反应的是( )
A、 稀硫酸 |
B、 稀硫酸 |
C、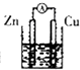 硫酸铜 |
D、 乙醇 |
在2mL 10%的硫酸铜溶液中滴加4~5滴2%的氢氧化钠溶液,再加入2mL 10%的葡萄糖溶液,加热,未观察到砖红色沉淀,最主要的原因是( )
| A、加热温度太高 |
| B、葡萄糖溶液中含有少量的果糖 |
| C、生成了氧化亚铜 |
| D、氢氧化钠不足 |
A的原子结构示意图为: ,其基态原子的价电子层电子排布式正确的是( )
,其基态原子的价电子层电子排布式正确的是( )
 ,其基态原子的价电子层电子排布式正确的是( )
,其基态原子的价电子层电子排布式正确的是( )| A、3s23p2 |
| B、3d24s2 |
| C、4s24p2 |
| D、3s23p4 |
下列物质的化学用语正确的是( )
A、甲烷分子的球棍模型 |
B、CO2的电子式: |
| C、乙酸的最简式:CH2O |
D、S2-的结构示意图: |
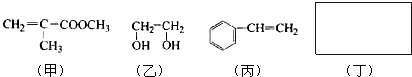
 利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是