题目内容
1.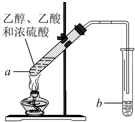 红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如下图所示的装置制取乙酸乙酯,请回答下列问题.
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如下图所示的装置制取乙酸乙酯,请回答下列问题.(1)该实验反应物与生成物有机物的官能团种类有羟基、羧基、酯基(填写名称).
(2)试管a中加入几块碎瓷片的目的是防止暴沸.
(3)试管a中发生反应的化学方程式为CH3COOH+C2H5OH$?_{加热}^{浓硫酸}$CH3COOC2H5+H2O,反应类型是酯化反应(取代反应).
(4)反应开始前,试管b中盛放的溶液是饱和碳酸钠溶液.作用是中和乙酸,吸收乙醇,降低乙酸乙酯的溶解度,有利于分层.
(5)反应结束后,振荡试管b,静置.反应结束后,试管b内的液体分成两层,乙酸乙酯在上层(填写“上”或“下”).若分离10mL该液体混合物需要用到的主要玻璃仪器是分液漏斗、烧杯.
分析 (1)乙醇与乙酸反应生成乙酸乙酯,乙醇中含-OH、乙酸中含-COOH、乙酸乙酯中含-COOC-;
(2)不加碎瓷片,加热时液体可能剧烈沸腾,液滴飞溅;
(3)试管a中发生酯化反应生成乙酸乙酯和水;
(4)试管b中为碳酸钠溶液,可吸收乙醇、除去乙酸,降低乙酸乙酯的溶解度;
(5)试管b内的液体分成两层,乙酸乙酯的密度小在上层,利用分液法分离.
解答 解:(1)乙醇与乙酸反应生成乙酸乙酯,乙醇中含-OH、乙酸中含-COOH、乙酸乙酯中含-COOC-,则官能团的名称分别为羟基、羧基、酯基,
故答案为:羟基、羧基、酯基;
(2)试管a中加入几块碎瓷片的目的是防止暴沸,故答案为:防止暴沸;
(3)试管a中发生反应的化学方程式为CH3COOH+C2H5OH$?_{加热}^{浓硫酸}$CH3COOC2H5+H2O,属于酯化反应(取代反应),
故答案为:CH3COOH+C2H5OH$?_{加热}^{浓硫酸}$CH3COOC2H5+H2O;酯化反应(取代反应);
(4)反应开始前,试管b中盛放的溶液是饱和碳酸钠溶液,其作用为中和乙酸,吸收乙醇,降低乙酸乙酯的溶解度,有利于分层,
故答案为:饱和碳酸钠溶液;中和乙酸,吸收乙醇,降低乙酸乙酯的溶解度,有利于分层;
(5)试管b内的液体分成两层,乙酸乙酯的密度小在上层,分离10mL该液体混合物选择分液法,需要用到的主要玻璃仪器是分液漏斗、烧杯,
故答案为:上;分液漏斗、烧杯.
点评 本题考查有机物的制备实验,为高频考点,侧重于学生的分析与实验能力的考查,把握有机物的结构与性质、有机制备原理是解答该题的关键,注意混合物分离提纯的应用,题目难度不大.

练习册系列答案
相关题目
10.1898年,居里夫人经过一段漫长、枯燥而又艰苦的工作,终于从数吨沥青铀矿中提炼出一小撮放射性粉末,并分离出了两种放射性元素钋和镭,其中镭是元素周期表中第7周期ⅡA族的元素.下列关于镭的性质描述中不正确的是( )
| A. | 在化合物中呈现+2价 | B. | 氢氧化物呈强碱性 | ||
| C. | 单质与冷水不反应 | D. | 碳酸盐难溶于水 |
11.光导纤维被广泛应用于光缆通讯,其主要成分是( )
| A. | CuO | B. | SiO2 | C. | Al2O3 | D. | Fe2O3 |
15.下列两种气体的分子数一定相同的是( )
| A. | 体积相等的SO2和CO2 | B. | 密度不同、质量相等的CO和C2H4 | ||
| C. | 等温等体积的NO和HCl | D. | 等压等体积的N2和CH4 |
6.下列物质肯定是纯净物的是( )
| A. | 汽油 | B. | 化学式为C2H6O的物质 | ||
| C. | 聚乙烯 | D. | 化学式为CH2Cl2的物质 |
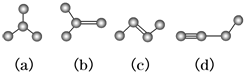

 C6H14
C6H14 C5H10
C5H10 C7H12
C7H12 C10H8.
C10H8. 金属钛冶炼过程中得到MgCl2,将熔融态MgCl2电解可得到金属镁和Cl2,氯气可制得漂白液、“84消毒液”等生活用品,试回答下列问题:
金属钛冶炼过程中得到MgCl2,将熔融态MgCl2电解可得到金属镁和Cl2,氯气可制得漂白液、“84消毒液”等生活用品,试回答下列问题: