题目内容
1.下列化学用语中正确的是( )| A. | CH2F2的电子式 | |
| B. | 对-硝基甲苯的结构简式  | |
| C. | 质子数为53、中子数为72的碘原子${\;}_{53}^{125}$I | |
| D. | 16O2与18O2互为同素异形体 |
分析 A.该电子式中漏掉了F原子最外层的3对未成键电子对;
B.硝基连接苯环原子应该是氮原子
C.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
D.二者都是氧气单质,不属于同素异形体.
解答 解:A.CH2F2的电子式中,F原子最外层达到8电子稳定结构,其正确的电子式为 ,故A错误;
,故A错误;
B.硝基中连接苯环的原子应该是氮原子,对-硝基甲苯的结构简式为: ,故B错误;
,故B错误;
C.质子数为53、中子数为72的碘原子的质量数为125,该原子可以表示为:${\;}_{53}^{125}$I,故C正确;
D.16O2与18O2为氧气单质,不属于同素异形体,故D错误;
故选C.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及结构简式、电子式、元素符号、同素异形体等知识,明确常见化学用语的书写原则即可解答,试题有利于提高学生的规范答题能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.下列对有机化合物的认识正确的是( )
| A. | 油脂不是高分子化合物,能发生水解反应 | |
| B. | 淀粉、纤维素的分子式都是(C6H10O5)n,二者互为同分异构体 | |
| C. | 一定条件下, 水解的产物只有 水解的产物只有  | |
| D. | .鸡蛋清溶液在硫酸铜溶液或饱和硫酸铵溶液中均会发生盐析 |
9.某学习小组为探究MnO2与FeCl3•6H2O的反应,设计了下列装置如图1:
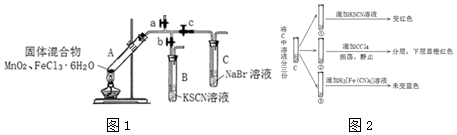
实验前查到信息:
①FeCl3熔点282℃,沸点315℃,FeCl3 $\frac{\underline{\;高温\;}}{\;}$ FeCl2+Cl2↑
②FeCl3•6H2O 熔点37℃,沸点285℃
实验过程记录:
回答下列问题:
(1)A中的白雾是盐酸小液滴.
(2)管壁内形成黄色液滴,可能的原因是FeCl3•6H2O受热气化,在管壁遇冷所致.
(3)B中溶液变红,用化学用语解释原因是Fe3++3SCN-=Fe(SCN)3.
(4)对C中溶液变黄色,小组展开进一步实验如图2:
Ⅰ.C中变黄的原因是Fe3+和Br2共同导致.
Ⅱ.C中发生反应的离子方程式是2Br-+Cl2=Br2+2Cl-.
(5)对A中残留物进行分离,其中得到一种不溶于水的红色固体,A中发生化学反应的方程式是3MnO2+4FeCl3•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+3MnCl2+3Cl2↑+24H2O.

实验前查到信息:
①FeCl3熔点282℃,沸点315℃,FeCl3 $\frac{\underline{\;高温\;}}{\;}$ FeCl2+Cl2↑
②FeCl3•6H2O 熔点37℃,沸点285℃
实验过程记录:
| 操作步骤 | 现象 |
| 1检查装置气密性,添加相应药品,点燃酒精灯,开始给A加热 | |
| 2打开a,关闭b、c,用湿润蓝色石蕊试纸贴近a口 | A中出现白雾,蓝色石蕊试纸变红 |
| 3打开b,关闭a、c | A中逐渐产生黄色气体,试管及导管壁内附有黄色液滴,B中溶液变红 |
| 4打开c,关闭a、b | C中溶液变棕黄色 |
| 5停止加热 |
(1)A中的白雾是盐酸小液滴.
(2)管壁内形成黄色液滴,可能的原因是FeCl3•6H2O受热气化,在管壁遇冷所致.
(3)B中溶液变红,用化学用语解释原因是Fe3++3SCN-=Fe(SCN)3.
(4)对C中溶液变黄色,小组展开进一步实验如图2:
Ⅰ.C中变黄的原因是Fe3+和Br2共同导致.
Ⅱ.C中发生反应的离子方程式是2Br-+Cl2=Br2+2Cl-.
(5)对A中残留物进行分离,其中得到一种不溶于水的红色固体,A中发生化学反应的方程式是3MnO2+4FeCl3•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+3MnCl2+3Cl2↑+24H2O.
16.下列实验与对应示意图的关系正确的是( )
| A | B | C | D |
| 向NaAlO2溶液中逐滴滴加盐酸至过量 | 向AlCl3溶液中逐滴滴加氨水至过量 | 向明矾溶液中逐滴滴加Ba(OH)2溶液至过量 | 向澄清石灰水中缓缓通入CO2至过量 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
13.氮化铝(AIN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO.下列叙述正确的是( )
| A. | 氮化铝中氮元素的化合价为+3 | |
| B. | AlN的摩尔质量为41g | |
| C. | 上述反应中每生成1molAlN,N2就得到3 mol电子 | |
| D. | 在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂 |
4.常温下在下列溶液中加入足量的铁,充分反应后,生成气体最多的是( )
| A. | 20mL 12mol•L-1的盐酸 | B. | 10mL 18mol•L-1的硫酸 | ||
| C. | 80mL 2mol•L-1的硫酸 | D. | 40mL 14mol•L-1的硝酸 |
5.在给定条件下,下列选项所示的物质间转化均能实现的是( )
| A. | MgCO3$\stackrel{HCl(aq)}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg | |
| B. | NaCl(aq)$\stackrel{CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| C. | Cu2(OH)2CO3$\stackrel{△}{→}$CuO$\stackrel{H_{2}O}{→}$Cu(OH)2 | |
| D. | SO2$\stackrel{氨水}{→}$NH4HSO3$\stackrel{H_{2}SO_{4}(aq)}{→}$(NH4)2SO4 |
 固体氧化物燃料电池的工作原理如图所示,已知电池中电解质为熔融固体氧化物,O2-可以在其中自由移动.当燃料气为C2H4时,其正极、负极反应式分别为
固体氧化物燃料电池的工作原理如图所示,已知电池中电解质为熔融固体氧化物,O2-可以在其中自由移动.当燃料气为C2H4时,其正极、负极反应式分别为
 +HNO3$\stackrel{浓硫酸}{→}$
+HNO3$\stackrel{浓硫酸}{→}$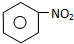 +H2O;③
+H2O;③ ;④
;④ .①③④均为取代反应(填反应类型).
.①③④均为取代反应(填反应类型). E
E .
.