题目内容
10.对于反应A2+3B2=2C来说,以下化学反应速率的表示中,反应速率最快的是( )| A. | v(B2)=4.8 mol/(L•min) | B. | v(A2)=1.5 mol/(L•s) | ||
| C. | v(C)=1.6 mol/(L•s) | D. | v(B2)=1.7 mol/(L•s) |
分析 由于不同物质表示的速率之比等于其化学计量数之比,则不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,注意单位要一致,据此进行解答.
解答 解:对于反应A2+3B2?2C,不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,
A.v(B2)=4.8 mol•L-1•min-1=0.08 mol•L-1•s-1,$\frac{1}{3}$v(B2)=$\frac{1}{3}$×0.08mol•L-1•s-1≈0.027mol•L-1•s-1;
B.v(A2)=1.5 mol•L-1•s-1=1.5mol•L-1•s-1;
C.$\frac{1}{2}$v(C)=$\frac{1}{2}$×1.6 mol•L-1•s-1=0.8mol•L-1•s-1;
D.$\frac{1}{3}$v(B2)=$\frac{1}{3}$×1.7mol•L-1•s-1≈0.57mol•L-1•s-1;
根据分析可知,反应速率最快的为B,
故选B.
点评 本题考查反应速率的比较,注意转化为同种物质的反应速率来比较,也可以利用反应速率与化学计量数的比值进行判断,比值越大,反应速率越快,难度不大.

练习册系列答案
相关题目
20.下列各组物质的性质变化正确的是( )
| A. | 酸性 HClO4>HNO3>H3PO4>H2SiO3 | B. | 稳定性H2S>HCl>HBr>HI | ||
| C. | 熔点 Rb>K>Na>Li | D. | 溶解性NaHCO3>Na2CO3>NaOH |
1.酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO2、ZnCl2和 NH4Cl 等组成的糊状填充物.该电池放电过程产生 MnOOH.回收处理该废电池可得到多种化工原料.有关数据如表所示溶解度/(g/100g 水)
回答下列问题:
(1)该电池的正极反应式为MnO2+H++e-=MnOOH,电池反应的离子方程式为2MnO2+Zn+2H+=2MnOOH+Zn2+;.
(2)废电池糊状填充物加水处理后,过滤,滤液中主要有 ZnCl2和NH4Cl,二者可通过加热浓缩、冷却结晶(填操作方法)分离回收;欲从滤渣中得到较纯的 MnO2,最简便的方法为在足量的空气或氧气中加热.
(3)用废电池的锌皮制备 ZnSO4•7H2O 的过程中,需除去锌皮中的少量杂质铁,其方法是:加稀 H2SO4和 H2O2溶解,铁变为Fe3+,加碱调节至 pH 为3时,铁刚好沉淀完全(离子浓度小于 1×10-5 mol•L-1时,即可认为该离子沉淀完全);继续加碱至 pH 为6时,锌开始沉淀(假定Zn2+浓度为0.1mol•L-1).若上述过程不加H2O2后果是Zn2+和Fe2+不能分离.
温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-38 |
(1)该电池的正极反应式为MnO2+H++e-=MnOOH,电池反应的离子方程式为2MnO2+Zn+2H+=2MnOOH+Zn2+;.
(2)废电池糊状填充物加水处理后,过滤,滤液中主要有 ZnCl2和NH4Cl,二者可通过加热浓缩、冷却结晶(填操作方法)分离回收;欲从滤渣中得到较纯的 MnO2,最简便的方法为在足量的空气或氧气中加热.
(3)用废电池的锌皮制备 ZnSO4•7H2O 的过程中,需除去锌皮中的少量杂质铁,其方法是:加稀 H2SO4和 H2O2溶解,铁变为Fe3+,加碱调节至 pH 为3时,铁刚好沉淀完全(离子浓度小于 1×10-5 mol•L-1时,即可认为该离子沉淀完全);继续加碱至 pH 为6时,锌开始沉淀(假定Zn2+浓度为0.1mol•L-1).若上述过程不加H2O2后果是Zn2+和Fe2+不能分离.
18.1828年德国化学家维勒从无机物制得了有机物,打破了只能从有机物取得有机物的学说,这种有机物是( )
| A. | 结晶牛胰岛素 | B. | 氰酸铵 | C. | 葡萄糖 | D. | 尿素 |
15.某同学探究第三周期元素性质递变规律,设计了下列实验方案.
(1)请你帮助该同学完成实验报告:
(2)综合以上实验,可以得到的实验结论:S>P.
(1)请你帮助该同学完成实验报告:
| 实验内容 | 实验现象 | 有关反应的方程式或结论 |
| ①取磨光后镁条与铝条,分别投入稀盐酸中 | Mg+2HCl=MgCl2+H2↓ 2Al+6HCl=2AlCl3+3H2↓ 说明金属性的强弱顺序为:Mg>Al | |
| ②向MgCl2、AlCl3溶液中分别逐滴滴入NaOH溶液至过量 | 与MgCl2溶液反应产生白色沉淀,与AlCl3溶液反应先产生白色沉淀,而后沉淀完全溶解 | AlCl3溶液与NaOH溶液反应的化学方程式:AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3+NaOH=NaAlO2+2H2O |
| ③向新制的Na2S溶液中滴入新制的氯水 | 生成淡黄色的沉淀 | 反应的化学方程式为:Na2S+Cl2=S↓+2NaCl |
| ④向各为1mol/L的H2SO4、H3PO4溶液中投入镁条 | 镁与H2SO4反应更剧烈,迅速产生大量无色气体 | 说明非金属性的强弱顺序为:S>P |
2.如表表格中各项分类都正确的一组是( )
类别 选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
| A | 生理盐水 | 明矾 | 液态KNO3 | 蔗糖 |
| B | CaO | 海 水 | 铜 | 乙醇 |
| C | 胆矾 | 铝合金 | AgCl | CO2 |
| D | 氢氧化钠 | 空气 | Na2SO4溶液 | 食醋 |
| A. | A | B. | B | C. | C | D. | D |
20.有7种物质:①甲烷;②苯;③聚乙烯;④聚异戊二烯;⑤2-丁炔;⑥环己烷;⑦环己烯.既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
| A. | ④⑤⑥⑦ | B. | ④⑤⑦ | C. | ②④⑤ | D. | ②④⑤⑦ |
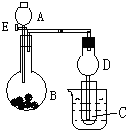 用如图所示装置进行实验,将A逐滴加入B中:
用如图所示装置进行实验,将A逐滴加入B中: