题目内容
0.1mol/L碳酸钠和0.1mol/L碳酸氢钠溶液的PH的大小关系为 .
考点:pH的简单计算,盐类水解的应用
专题:盐类的水解专题
分析:等浓度的强碱弱酸盐溶液水解程度大于其酸式弱酸盐溶液的水解程度.
解答:
解:等浓度的弱酸盐溶液水解程度大于其酸式弱酸盐溶液的水解程度,水解程度越大,碱性越强,PH越大.故答案为:碳酸钠>碳酸氢钠.
点评:本题考查了强碱弱酸盐的水解程度大小比较问题,注意水解程度地影响因素,难度不大.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
Mg(OH)2在下列四种情况下,其溶解度最大的是( )
| A、在纯水中 |
| B、在0.1 mol?L-1的CH3COOH溶液中 |
| C、在0.1 mol?L-1的NH3?H2O溶液中 |
| D、在0.1 mol?L-1的MgCl2溶液中 |
强酸与强碱的稀溶液发生中和反应的热化学方程式为:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,分别向1L 0.5mol/L的NaOH溶液中加入:①稀醋酸;②浓H2SO4;③稀硝酸.恰好完全反应时的热效应分别为△H1、△H2、△H3,它们的关系正确的是( )
| A、△H1>△H2>△H3 |
| B、△H2>△H3>△H1 |
| C、△H1=△H2=△H3 |
| D、△H1>△H3>△H2 |
 如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得两个装置中均通过0.02mol电子时(不考虑盐的水解和溶液体积的变化)则下列叙述中正确的是( )
如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得两个装置中均通过0.02mol电子时(不考虑盐的水解和溶液体积的变化)则下列叙述中正确的是( )| A、电极上析出物质的质量:①=② |
| B、溶液的pH变化:①增大,②不变 |
| C、电极反应式:①中阳极 2Cl--2e-═Cl2↑ ②中负极 2H++2e-═H2↑ |
| D、产生气体的体积:①=② |
下列变化中,一定不存在化学能与热能相互转化的是( )
| A、酸碱中和反应 | B、白磷自燃 |
| C、燃放爆竹 | D、干冰气化 |
下列说法中正确的是(NA代表阿伏伽德罗常数)( )
| A、28g N2和28g CO所含的分子数都是NA |
| B、32g O3和32g O2所含的分子数都是NA |
| C、28g CO和44g CO2所含的氧原子数都是2NA |
| D、98g H2SO4和98g H3PO4所含的氧原子数都是4NA |
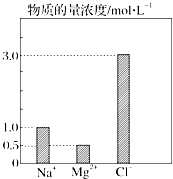 在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示.
在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示.