题目内容
在一密闭容器中,反应 aA(g) bB(g)+cC(g)达平衡后,保持温度不变,将容器体积增加一倍,最终测得A的物质的量的浓度变为原来的50%,则
bB(g)+cC(g)达平衡后,保持温度不变,将容器体积增加一倍,最终测得A的物质的量的浓度变为原来的50%,则
A.平衡向正反应方向移动 B.a>(b+c)
C.物质B的质量分数增大 D.以上判断都错误
练习册系列答案
相关题目
3.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,11.2L CHCl3含有的原子总数为2.5NA | |
| B. | 25g质量分数为68%的H2O2溶液中含有氧原子数目为NA | |
| C. | 高温下,16.8gFe与足量水蒸气完全反应失去0.8NA个电子 | |
| D. | 1molCH5+中含有的电子数目为11NA |
13.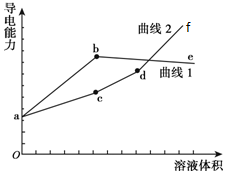 分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )
分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )
 分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )
分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )| A. | 曲线1代表滴加NaOH溶液的变化曲线 | |
| B. | C点溶液中大量存在的离子是Na+和SO42- | |
| C. | b和d点对应的溶液均显酸性 | |
| D. | be段导电能力下降的原因是NH3•H2O?NH4++OH-,导致离子数目减少 |


 zC达到平衡时,请填写:
zC达到平衡时,请填写:
 6A+2C
6A+2C H2O(l)ΔH=57.3KJ·mol-1
H2O(l)ΔH=57.3KJ·mol-1