题目内容
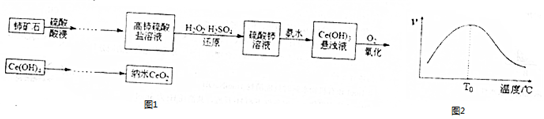
4.氯化亚铜(CuCl)是白色粉末,不溶于水、乙醇及稀硫酸,在空气中迅速被氧化成绿色,常用作有机合成工业中的催化剂.实验室拟以下列方法制取CuCl:在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl.试回答以下问题:(1)CuCl制备过程中需配制物质的量浓度为2.0mol/L的CuSO4溶液.配制950mL 2.0mol/L的CuSO4溶液应称取胆矾的质量为500 g.
(2)写出用上述方法制备CuCl的离子方程式2Cu2++SO32-+2Cl-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl↓+SO42-+2H+.
(3)在上述制取过程中,经过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却,密封包装即得产品.其中“于70℃真空干燥”的目的是防止CuCl被空气氧化(或加快乙醇和水的蒸发).(回答一点)
(4)据世界卫生组织统计,最常用的避孕环含金属铜,避孕过程中生成了CuCl.其原因是铜与人体分泌物中的盐酸以及子宫内的空气反应:Cu+HCl+O2=CuCl+HO2,HO2(超氧酸) 不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列有关说法或表示正确的是C.
A.氧化产物是HO2
B.HO2在碱中能稳定存在
C.HO2 的电离方程式是HO2?H++O2-
D.1mol O2 参加反应有4mol电子发生转移.
分析 (1)一定容积规格的容量瓶只能配制相应体积的溶液,由于没有950ml的容量瓶,选择大于950ml相近规格的容量瓶;根据化学式可知硫酸铜的物质的量等于硫酸铜晶体的物质的量,根据m=cnM计算所需胆矾的质量;
(2)亚硫酸根和硫酸铜之间可以发生氧化还原反应生成氯化亚铜沉淀;
(3)乙醇和水易挥发,CuCl具有还原性,可以被空气氧化;
(4)反应Cu+HCl+O2=CuCl+HO2中Cu元素化合价升高,被氧化,O元素化合价降低,被还原,O2为氧化剂,结合元素化合价的变化解答该题.
解答 解:(1)由于没有950ml的容量瓶,选择大于950ml相近规格的容量瓶,所以应选择1000ml规格容量瓶,
根据化学式可知硫酸铜的物质的量等于硫酸铜晶体的物质的量,所以需要胆矾的质量为:
1L×2mol/L×250g/mol=500g,
故答案为:500;
(2)Na2SO3和硫酸铜之间可以发生氧化还原反应生成氯化亚铜沉淀,反应的离子方程式为:2Cu2++SO32-+2Cl-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl↓+SO42-+2H+,
故答案为:2Cu2++SO32-+2Cl-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl↓+SO42-+2H+;
(3)CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,这样可以加快乙醇和水的蒸发,防止CuCl被空气氧化,
故答案为:防止CuCl被空气氧化(或加快乙醇和水的蒸发);
(4)A.O元素化合价降低,被还原,HO2为还原产物,故A错误;
B.HO2为超氧酸,应具有酸性,可与碱反应,故B错误;
C.HO2(超氧酸) 是一种弱酸,所以HO2 的电离方程式为HO2?H++O2-,故C正确;
D.反应中Cu元素化合价由0价升高到+1价,则1molCu参加反应有1mol电子发生转移,故D错误.
故选C.
点评 本题考查了配制一定物质的浓度溶液的配制、铜及其化合物的性质,注意知识的迁移和应用,掌握氧化还原知识以及铜的化合物的性质是解题关键,题目难度中等.

| A. | 原子半径:X>Y>W>Z | B. | 原子序数:Y>X>Z>W | ||
| C. | 原子最外层电子数:Y>X>Z>W | D. | 原子的电子层数:X=Y>W=Z |
| A. | 等于0.1mol/L | B. | 大于0.1mol/L | C. | 小于0.1mol/L | D. | 无法判断 |
(1)常温下,将pH=3的盐酸a L分别与下列三种溶液混合,结果溶液均呈中性.①浓度为1.0×10-3 mol•L-1的氨水b L;②c(OH-)=1.0×10-3 mol•L-1的氨水c L;③c(OH-)=1.0×10-3 mol•L-1的氢氧化钡溶液d L.
则a、b、c、d之间的关系是b>a=d>c.
(2)已知:Ksp(AgCl)=1.8×10-10,向50mL 0.018mol•L-1的AgNO3溶液中加入相同体积0.020mol•L-1的盐酸,则①c(Ag+)=1.8×10-7mol/L,②此时所得混合溶液的pH=2.
(3)常温下,浓度均为0.1mol•L-1的下列六种溶液的pH如表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | NaX |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
②根据表中数据,浓度均为0.01mol•L-1的下列五种物质的溶液中,分别稀释100倍,pH变化最小的是C(填编号).
A、HCN B、HClO C、HX D、CH3COOH E、H2CO3
③据上表数据,请你判断下列反应不能成立的是BD(填编号).
A.2CH3COOH+Na2CO3═CO2+H2O+2CH3COONa
B.HClO+HCO3-═ClO-+CO2+H2O
C.CH3COOH+NaCN═CH3COONa+HCN
D.CO2+H2O+2NaX═Na2CO3+2HX
(4)将NaHCO3溶液与FeCl3溶液混合,反应的离子方程式是:Fe3++3HCO3-=Fe(OH)3↓+3CO2↑.

| A. | a1℃时甲和乙的饱和溶液,升温到a2℃时仍是饱和溶液 | |
| B. | 甲和乙的溶解度相等 | |
| C. | a1℃时,甲和乙各30g分别加入100g的水中,均形成饱和溶液 | |
| D. | a2℃时,在100g水中加入60g甲,形成不饱和溶液 |
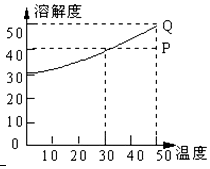 有一种盐的溶解度曲线如图,现有组成处于P点上的该溶液,下列说法错误的是(此盐不含结晶水)( )
有一种盐的溶解度曲线如图,现有组成处于P点上的该溶液,下列说法错误的是(此盐不含结晶水)( )| A. | 50℃时,若该盐溶液含A克溶质,保持温度不变,加入A/4 g溶质,溶液必变成饱和溶液 | |
| B. | 50℃时,140g P点溶液最少需蒸发掉20g水才能形成饱和溶液 | |
| C. | 该溶液冷却至0℃时,析出溶质10 g | |
| D. | 在保持溶质及溶剂质量不变的情况下,使P点溶液达到饱和需降温20℃ |
 ;
;