题目内容
4.某一元弱酸溶液的c(H+)=0.1mol/L,该酸溶液的物质的量浓度为( )| A. | 等于0.1mol/L | B. | 大于0.1mol/L | C. | 小于0.1mol/L | D. | 无法判断 |
分析 弱酸为弱电解质,部分电离,据此分析解答.
解答 解:弱酸为弱电解质,部分电离,某一元弱酸溶液的c(H+)=0.1mol/L,则该一元弱酸的物质的量浓度大于0.1mol/L;
故选:B.
点评 本题以物质的量浓度计算为载体考查了弱电解质的电离,注重了基础知识的考查,把握弱电解质部分电离是解题关键,题目难度较低.

练习册系列答案
相关题目
19.下列有关实验叙述不正确的是( )
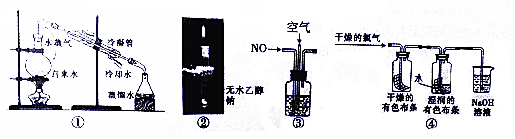

| A. | 图①用于除去自来水中的Fe3+、C1-等杂质离子 | |
| B. | 图②中直接点燃气体,证明钠与乙醇反应的气体产物是H2 | |
| C. | 图③在探究NO充分转化成HNO3的实验中,观察气泡速率控制通入气体体积比 | |
| D. | 图④用该实验可以证明Cl2体现漂白作用的原因 |
11.相等物质的量的CO和CO2相比较,下列比较中正确的是( )
①它们所含的分子数目之比为1:1
②它们所含的氧原子数目之比为1:1
③它们所含的原子总数目之比为2:3
④它们所含的碳原子数目之比为1:1.
①它们所含的分子数目之比为1:1
②它们所含的氧原子数目之比为1:1
③它们所含的原子总数目之比为2:3
④它们所含的碳原子数目之比为1:1.
| A. | ①② | B. | ②③ | C. | ①②④ | D. | ①③④ |
8.在下列溶液中分别放入铁棒,过一会儿把铁棒取出,(1)能使铁棒质量增加的溶液是____;(2)溶液质量增加的是______.( )
| A. | 稀硫酸 | B. | 食盐水 | C. | 硫酸铜溶液 | D. | 乙醇水溶液 |
 ;
;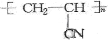 .
.
 ;
;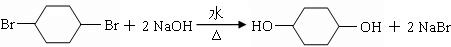 .
.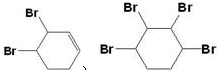 .
.