题目内容
A~D是原子序数在20以内的元素,其性质或结构信息如下表
请根据表中的信息回答下列问题:
(1)A离子的结构示意图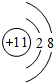
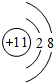 ,B原子的电子式
,B原子的电子式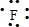
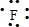 ,C的单质的电子式为
,C的单质的电子式为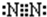
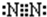 .
.
(2)和B的氢化物所含电子数相同的4种微粒有
(3)C的气态氢化物的水化物的电离方程式:
(4)对应离子半径大小比较:A
| 元素 | A | B | C | D |
| 性质或 结构信息 |
其单质和化合物的焰色均为黄色 | 其氢化物的水溶液能腐蚀玻璃 | 其单质在空气中体积含量最多 | 地壳中含量最多的金属元素 |
(1)A离子的结构示意图
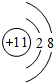
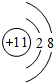
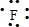
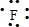
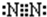
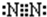
(2)和B的氢化物所含电子数相同的4种微粒有
H2O
H2O
,NH3
NH3
,CH4
CH4
,OH-
OH-
.(3)C的气态氢化物的水化物的电离方程式:
NH3?H2O?NH4++OH-
NH3?H2O?NH4++OH-
.(4)对应离子半径大小比较:A
>
>
D.分析:A~D是原子序数在20以内的元素:A的单质和化合物的焰色均为黄色,则A为Na;B的氢化物的水溶液能腐蚀玻璃,则B为F;C的单质在空气中体积含量最多,则C为N;D元素是地壳中含量最多的金属元素,则D为Al,然后根据问题回答.
解答:解:A~D是原子序数在20以内的元素:A的单质和化合物的焰色均为黄色,则A为Na;B的氢化物的水溶液能腐蚀玻璃,则B为F;C的单质在空气中体积含量最多,则C为N;D元素是地壳中含量最多的金属元素,则D为Al,
(1)Na+的结构示意图为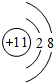 ,F原子电子式为
,F原子电子式为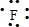 ,N2的电子式为
,N2的电子式为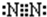 ,
,
故答案为: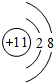 ;
;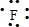 ;
;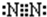 ;
;
(2)HF中所含电子数为10,常见的10电子粒子有:Ne、H2O、NH3、CH4、OH-、F-、O2-、N3-、Na+、Mg2+、Al3+、H3O+、NH4+
故答案为:Ne、H2O、NH3、CH4、OH-、F-、O2-、N3-、Na+、Mg2+、Al3+、H3O+、NH4+(其中的任意4项均可)
(3)NH3与水化合为NH3?H2O,在溶液中发生电离NH3?H2O?NH4++OH-,
故答案有:NH3?H2O?NH4++OH-;
(4)Na+、Al3+电子层结构相同,核电荷数越大离子半径越小,故离子半径Na+>Al3+,
故答案为:>.
(1)Na+的结构示意图为
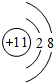 ,F原子电子式为
,F原子电子式为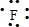 ,N2的电子式为
,N2的电子式为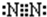 ,
,故答案为:
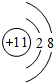 ;
;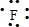 ;
;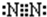 ;
; (2)HF中所含电子数为10,常见的10电子粒子有:Ne、H2O、NH3、CH4、OH-、F-、O2-、N3-、Na+、Mg2+、Al3+、H3O+、NH4+
故答案为:Ne、H2O、NH3、CH4、OH-、F-、O2-、N3-、Na+、Mg2+、Al3+、H3O+、NH4+(其中的任意4项均可)
(3)NH3与水化合为NH3?H2O,在溶液中发生电离NH3?H2O?NH4++OH-,
故答案有:NH3?H2O?NH4++OH-;
(4)Na+、Al3+电子层结构相同,核电荷数越大离子半径越小,故离子半径Na+>Al3+,
故答案为:>.
点评:本题考查原子结构与元素周期律的关系,题目难度不大,正确推断元素的种类是解答本题的关键,然后根据元素化合物知识进行解答.

练习册系列答案
相关题目
A~D是原子序数在20以内的元素,其性质或结构信息如下表
请根据表中的信息回答下列问题:
(1)A离子的结构示意图 ,B原子的电子式 ,C的单质的电子式为 .
(2)和B的氢化物所含电子数相同的4种微粒有 , , , .
(3)C的气态氢化物的水化物的电离方程式: .
(4)对应离子半径大小比较:A D.
| 元素 | A | B | C | D |
| 性质或 结构信息 | 其单质和化合物的焰色均为黄色 | 其氢化物的水溶液能腐蚀玻璃 | 其单质在空气中体积含量最多 | 地壳中含量最多的金属元素 |
(1)A离子的结构示意图 ,B原子的电子式 ,C的单质的电子式为 .
(2)和B的氢化物所含电子数相同的4种微粒有 , , , .
(3)C的气态氢化物的水化物的电离方程式: .
(4)对应离子半径大小比较:A D.
A~D是原子序数在20以内的元素,其性质或结构信息如下表
请根据表中的信息回答下列问题:
(1)A离子的电子排布式为______,B原子核外电子的轨道表示式为______.
(2)和B的氢化物所含电子数相同的4种粒子有______.
(3)C的单质特别稳定,原因在于______.C的气态氢化物的水溶液中存在的平衡:______.
(4)工业上制取 D的单质的化学方程式为______ 4Al+3O2↑
| 元素 | A | B | C | D |
| 性质 或 结构 信息 | 其单质和化合物的焰色均为黄色 | 其氢化物的水溶液能腐蚀玻璃 | 湿润的红色石蕊试纸遇其最低价氢化物变蓝 | 其原子核外有13种运动状态的电子 |
(1)A离子的电子排布式为______,B原子核外电子的轨道表示式为______.
(2)和B的氢化物所含电子数相同的4种粒子有______.
(3)C的单质特别稳定,原因在于______.C的气态氢化物的水溶液中存在的平衡:______.
(4)工业上制取 D的单质的化学方程式为______ 4Al+3O2↑

