题目内容
高温焙烧含硫废渣会产生SO2废气,为了回收利用SO2,研究人员研制了利用低品位软锰矿浆(主要成分是MnO2)吸收SO2,并制备硫酸锰晶体的生产流程,其流程示意图如下:

已知,浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子.有关金属离子形成氢氧化物沉淀时的pH见表:
请回答下列问题:
(1)高温焙烧:在实验室宜选择的主要仪器是 .
(2)写出氧化过程中主要反应的离子方程式: .
(3)在氧化后的液体中加入石灰浆,并调节溶液pH,pH应调节的范围是 .
(4)滤渣的主要成分有 .
(5)工业生产中为了确定需要向浸出液中加入多少MnO2粉,可准确量取l0.00mL浸出液用0.02mol/L酸性KMnO4溶液滴定,判断滴定终点的方法是 ;若达滴定终点共消耗l0.00mL酸性KMnO4溶液,请计算浸出液中Fe2+浓度是 .
(6)操作a的具体过程 .

已知,浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子.有关金属离子形成氢氧化物沉淀时的pH见表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
(1)高温焙烧:在实验室宜选择的主要仪器是
(2)写出氧化过程中主要反应的离子方程式:
(3)在氧化后的液体中加入石灰浆,并调节溶液pH,pH应调节的范围是
(4)滤渣的主要成分有
(5)工业生产中为了确定需要向浸出液中加入多少MnO2粉,可准确量取l0.00mL浸出液用0.02mol/L酸性KMnO4溶液滴定,判断滴定终点的方法是
(6)操作a的具体过程
考点:制备实验方案的设计,难溶电解质的溶解平衡及沉淀转化的本质,二氧化硫的化学性质
专题:实验题
分析:高温焙烧含硫废渣产生的SO2废气,软锰矿浆的主要成分是MnO2,通入SO2浸出液的pH<2,其中的金属离子主要是Mn2+,则MnO2与SO2发生氧化还原反应,浸出液还含有少量的Fe2+、Al3+等其他金属离子,Fe2+具有还原性,可以被MnO2在酸性条件下氧化成Fe3+,在氧化后的液体中加入石灰浆,杂质中含有Fe2+、Al3+、Ca2+等阳离子,由沉淀的pH范围知,Fe2+的沉淀与Mn2+离子的沉淀所需的pH接近,而Fe3+则相差很远,故可以将Fe2+氧化成Fe3+而除杂.调节pH值在4.7~8.3间,Fe3+、Al3+阳离子通过调pH值,转化为氢氧化铁、氢氧化铝沉淀,同时生成微溶的硫酸钙,过滤,滤渣主要有氢氧化铁、氢氧化铝、硫酸钙,由于制取的MnSO4?H2O含有结晶水,故操作a采用蒸发浓缩结晶的方法,得到MnSO4?H2O.
(1)加热固体,应在坩埚中进行;
(2)杂质离子中只有Fe2+具有还原性,可以被MnO2在酸性条件下氧化成Fe3+;
(3)从表可以看出,只要调节pH值在4.7~8.3间,大于4.7可以将Fe3+和Al3+除去,小于8.3是防止Mn2+也沉淀;
(4)Fe3+、Al3+阳离子通过调pH值,转化为氢氧化铁、氢氧化铝沉淀,同时生成微溶的硫酸钙;
(5)高锰酸钾有颜色,滴定终点时溶液变为紫红色,结合电子转移的数目计算;
(6)由滤液得到晶体,应进行蒸发浓缩、冷却结晶、过滤洗涤等操作.
(1)加热固体,应在坩埚中进行;
(2)杂质离子中只有Fe2+具有还原性,可以被MnO2在酸性条件下氧化成Fe3+;
(3)从表可以看出,只要调节pH值在4.7~8.3间,大于4.7可以将Fe3+和Al3+除去,小于8.3是防止Mn2+也沉淀;
(4)Fe3+、Al3+阳离子通过调pH值,转化为氢氧化铁、氢氧化铝沉淀,同时生成微溶的硫酸钙;
(5)高锰酸钾有颜色,滴定终点时溶液变为紫红色,结合电子转移的数目计算;
(6)由滤液得到晶体,应进行蒸发浓缩、冷却结晶、过滤洗涤等操作.
解答:
解:高温焙烧含硫废渣产生的SO2废气,软锰矿浆的主要成分是MnO2,通入SO2浸出液的pH<2,其中的金属离子主要是Mn2+,则MnO2与SO2发生氧化还原反应,浸出液还含有少量的Fe2+、Al3+等其他金属离子,Fe2+具有还原性,可以被MnO2在酸性条件下氧化成Fe3+,在氧化后的液体中加入石灰浆,杂质中含有Fe2+、Al3+、Ca2+等阳离子,由沉淀的pH范围知,Fe2+的沉淀与Mn2+离子的沉淀所需的pH接近,而Fe3+则相差很远,故可以将Fe2+氧化成Fe3+而除杂.调节pH值在4.7~8.3间,Fe3+、Al3+阳离子通过调pH值,转化为氢氧化铁、氢氧化铝沉淀,同时生成微溶的硫酸钙,过滤,滤渣主要有氢氧化铁、氢氧化铝、硫酸钙,由于制取的MnSO4?H2O含有结晶水,故操作a采用蒸发浓缩结晶的方法,得到MnSO4?H2O.
(1)加热固体,应在坩埚中进行,故答案为:坩埚;
(2)杂质离子中只有Fe2+具有还原性,可以被MnO2在酸性条件下氧化成Fe3+,反应的离子方程式为2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O,
故答案为:2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O;
(3)杂质中含有Fe3+、Al3+阳离子,从图可表以看出,大于4.7可以将Fe3+和Al3+除去,小于8.3是防止Mn2+也沉淀,所以只要调节pH值在4.7~8.3间即可,
故答案为:4.7≤pH<8.3;
(4)Fe3+、Al3+阳离子通过调pH值,转化为氢氧化铁、氢氧化铝沉淀,同时生成微溶的硫酸钙,所以滤渣主要有氢氧化铁、氢氧化铝、硫酸钙,
故答案为:氢氧化铁、氢氧化铝、硫酸钙;
(5)高锰酸钾有颜色,滴定终点时溶液变为紫红色,判断方法为当滴入最后一滴酸性KMnO4溶液,溶液变紫红色,且半分钟内不褪色,若达滴定终点共消耗l0.00mL酸性KMnO4溶液,则n(KMnO4)=0.01L×0.02mol/L=2×10-4mol,得电子的物质的量为2×10-4mol×(7-2)=10-3mol,反应中Fe2+被氧化生成Fe3+,则
n(Fe2+)=10-3mol,c(Fe2+)=
=0.1 mol/L
故答案为:当滴入最后一滴酸性KMnO4溶液,溶液变紫红色,且半分钟内不褪色;0.1 mol/L;
(6)由滤液得到晶体,应进行蒸发浓缩、冷却结晶、过滤洗涤等操作,故答案为:蒸发浓缩、冷却结晶、过滤洗涤.
(1)加热固体,应在坩埚中进行,故答案为:坩埚;
(2)杂质离子中只有Fe2+具有还原性,可以被MnO2在酸性条件下氧化成Fe3+,反应的离子方程式为2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O,
故答案为:2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O;
(3)杂质中含有Fe3+、Al3+阳离子,从图可表以看出,大于4.7可以将Fe3+和Al3+除去,小于8.3是防止Mn2+也沉淀,所以只要调节pH值在4.7~8.3间即可,
故答案为:4.7≤pH<8.3;
(4)Fe3+、Al3+阳离子通过调pH值,转化为氢氧化铁、氢氧化铝沉淀,同时生成微溶的硫酸钙,所以滤渣主要有氢氧化铁、氢氧化铝、硫酸钙,
故答案为:氢氧化铁、氢氧化铝、硫酸钙;
(5)高锰酸钾有颜色,滴定终点时溶液变为紫红色,判断方法为当滴入最后一滴酸性KMnO4溶液,溶液变紫红色,且半分钟内不褪色,若达滴定终点共消耗l0.00mL酸性KMnO4溶液,则n(KMnO4)=0.01L×0.02mol/L=2×10-4mol,得电子的物质的量为2×10-4mol×(7-2)=10-3mol,反应中Fe2+被氧化生成Fe3+,则
n(Fe2+)=10-3mol,c(Fe2+)=
| 10-3mol |
| 0.01L |
故答案为:当滴入最后一滴酸性KMnO4溶液,溶液变紫红色,且半分钟内不褪色;0.1 mol/L;
(6)由滤液得到晶体,应进行蒸发浓缩、冷却结晶、过滤洗涤等操作,故答案为:蒸发浓缩、冷却结晶、过滤洗涤.
点评:本题以制备硫酸锰的生产流程为知识载体,综合考查学生的分析能力、实验能力和计算能力,为高频考点,涉及考查化学反应的书写,及除杂中的问题,题目难度中等,本题注意把握数据处理能力和图象分析能力.

练习册系列答案
相关题目
下列有机化学方程式书写不正确的是( )
A、CH2CH=CH2+Br2→CH3- | |||
B、 +HNO3 +HNO3
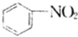 +H2O +H2O | |||
C、2CH3CH2OH+O2
| |||
D、CH3CH2OH+CH3COOH
|
下列化合物在核磁共振氢谱中能出现两组峰.且其峰面积之比为3:1的有( )
| A、乙酸异丙酯 |
| B、甲酸叔丁酯 |
| C、对二甲苯 |
| D、1,3,5-三甲苯 |
 由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀,若用如图所示实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁.
由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀,若用如图所示实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁.