题目内容
下表是素周期表的一部分,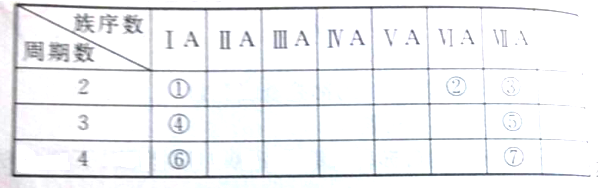
(1)②、④、⑤的元素符号是 、 、
(2)表中最活泼的金属元素是 ,非金属性最强的元素是 (填写元素符号).
(3)④与水发生反应的化学方程式是
(4)请设计一个实验方案,比较⑤、⑦单质氧化性强弱 .

(1)②、④、⑤的元素符号是
(2)表中最活泼的金属元素是
(3)④与水发生反应的化学方程式是
(4)请设计一个实验方案,比较⑤、⑦单质氧化性强弱
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中的位置可知①②③④⑤⑥⑦分别为Li、O、F、Na、Cl、K、Br,结合金属性、非金属性的递变规律解答,可根据单质之间的置换反应比较氧化性强弱,以此解答该题.
解答:
解:由元素在周期表中的位置可知①②③④⑤⑥⑦分别为Li、O、F、Na、Cl、K、Br,
(1)②、④、⑤的元素符号是O、Na、Cl,故答案为:O;Na;Cl;
(2)元素周期表中,同周期元素从左到右,元素的金属性逐渐减弱,非金属性逐渐增强,同主族元素从上到下,元素的金属性逐渐增强,非金属性逐渐减弱,则表中最活泼的金属元素是K,非金属性最强的元素是F,故答案为:K;F;
(3)④为Na,与水反应生成氢氧化钠和氢气,反应的化学方程式为2Na+2H2O=2NaOH+H2↑,故答案为:2Na+2H2O=2NaOH+H2↑;
(4)元素⑤为氯,元素⑦为溴,氯单质将溴离子氧化为溴单质就能证明氯化溴的氧化性强.将氯水加入到溴化钠溶液中,有红棕色的Br2生成,证明单质氯比单质溴氧化性强,故答案为:在NaBr溶液中滴加Cl2水,若溶液加深(有红棕色形成),说明Cl2的氧化性比Br2强.
(1)②、④、⑤的元素符号是O、Na、Cl,故答案为:O;Na;Cl;
(2)元素周期表中,同周期元素从左到右,元素的金属性逐渐减弱,非金属性逐渐增强,同主族元素从上到下,元素的金属性逐渐增强,非金属性逐渐减弱,则表中最活泼的金属元素是K,非金属性最强的元素是F,故答案为:K;F;
(3)④为Na,与水反应生成氢氧化钠和氢气,反应的化学方程式为2Na+2H2O=2NaOH+H2↑,故答案为:2Na+2H2O=2NaOH+H2↑;
(4)元素⑤为氯,元素⑦为溴,氯单质将溴离子氧化为溴单质就能证明氯化溴的氧化性强.将氯水加入到溴化钠溶液中,有红棕色的Br2生成,证明单质氯比单质溴氧化性强,故答案为:在NaBr溶液中滴加Cl2水,若溶液加深(有红棕色形成),说明Cl2的氧化性比Br2强.
点评:关于元素周期律的考题一般难度都不大,做好该类型题目的关键是要准.要在头脑中有一个完整准确的元素周期表,这样就能准确判断元素,尽而回答出相关的问题.该题设计实验虽然简单,但体现了新课标的要求.

练习册系列答案
相关题目
下列说法错误的是( )
| A、氯气是黄绿色的,氯离子是无色的 |
| B、氢气在氯气中燃烧时发出苍白色火焰 |
| C、氯气有毒,新制的氯水有漂白性,而氯离子既无毒也无漂白性 |
| D、氢气和氯气的混合气体只有在强光照射下才能迅速化合生成氯化氢 |
下列反应的离子方程式正确的是( )
| A、铁和足量稀硝酸反应 Fe+2H+═Fe2++H2↑ | ||||
B、氯化铁溶液滴入沸水 Fe3++3H2O
| ||||
| C、硝酸银溶液中滴入食盐水 Cl-+Ag+═AgCl↓ | ||||
| D、氯气通入烧碱溶液 Cl2+2OH-═Cl-+ClO-+H2O |
下列装置或操作能达到目的是( )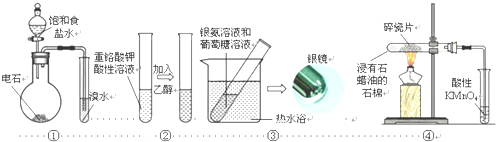

| A、装置①:制取乙炔并验证炔烃的性质 |
| B、装置②:检验乙醇的氧化性,溶液颜色从绿色变成橙色 |
| C、装置③:验证葡萄糖分子中含有醛基官能团 |
| D、装置④:酸性KMnO4溶液中出现气泡且颜色逐渐褪去 |
下列气体不能用浓H2SO4干燥的是( )
| A、CO2 |
| B、H2S |
| C、SO2 |
| D、HCl |

 为原料制备
为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2Br
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2Br