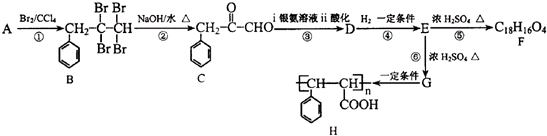
题目内容
下列化学用语正确的是( )
A、NaF的电子式[:
| ||||
| B、乙醇的结构简式C2H6O | ||||
C、铝的原子结构示意图 | ||||
| D、硫酸的电离方程式H2SO4═H22++SO42- |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氟离子为阴离子,其电子式漏掉了标出最外层的8个电子;
B.乙醇中含有官能团羟基,结构简式中需要标出其官能团;
C.铝原子的核电荷数=核外电子总数=13,最外层为3个电子;
D.硫酸的电离的两个氢离子不能合并,应该拆开写.
B.乙醇中含有官能团羟基,结构简式中需要标出其官能团;
C.铝原子的核电荷数=核外电子总数=13,最外层为3个电子;
D.硫酸的电离的两个氢离子不能合并,应该拆开写.
解答:
解:解:A.氟化钠中存在阴阳离子,钠离子用离子符号表示,氟离子需要表示出所带电荷及最外层电子,正确的电子式为: ,故A错误;
,故A错误;
B.乙醇的官能团为羟基,乙醇的结构简式为:CH3CH2OH,故B错误;
C.氯原子核电荷数为13,核外电子数也是13,所以铝的原子结构示意图: ,故C正确;
,故C正确;
D.硫酸为强电解质,硫酸正确的电离方程式为:H2SO4═2H++SO42-,故D错误;
故选C.
 ,故A错误;
,故A错误;B.乙醇的官能团为羟基,乙醇的结构简式为:CH3CH2OH,故B错误;
C.氯原子核电荷数为13,核外电子数也是13,所以铝的原子结构示意图:
 ,故C正确;
,故C正确;D.硫酸为强电解质,硫酸正确的电离方程式为:H2SO4═2H++SO42-,故D错误;
故选C.
点评:本题考查了电子式、电离方程式、原子结构示意图的判断,题目难度中等,注意掌握电子式、原子结构示意图等化学用语的表示方法,明确离子化合物与共价化合物的电子式区别.

练习册系列答案
相关题目
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如下处理:下列说法正确的是( )


| A、滤液A中的阳离子为Fe2+、Fe3+、H+ |
| B、样品中Fe元素的质量为1.12 g |
| C、样品中CuO的质量为4.0 g |
| D、V=448 |
下列关于氧化还原反应的说法,正确的是( )
| A、氧化还原反应的特征是电子的转移 |
| B、氧化剂在反应中被还原,生成氧化产物 |
| C、同一反应中,氧化剂得电子的总数一定等于还原剂失电子的总数 |
| D、任何反应中一定有氧化剂和还原剂,且氧化剂和还原剂可以为同种物质 |
“纳米材料”是粒子直径为1~100nm(纳米)的材料,纳米碳就是其中的一种.若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )①是溶液 ②是胶体 ③能透过滤纸 ④不能透过滤纸 ⑤能产生丁达尔效应 ⑥静置后,会析出黑色沉淀.
| A、①④⑥ | B、②③④ |
| C、②③⑤ | D、①③④⑥ |
反应:aX(g)+bY(g)?cZ(g),达到平衡时测得X气体的浓度为1mol/L,在恒温下将该容器体积扩大一倍,再次达到平衡时,测得X气体的浓度为0.6mol/L,则下列叙述正确的是( )
| A、a+b<c |
| B、平衡向生成Z的方向移动 |
| C、Z的体积分数降低 |
| D、Y的转化率升高 |
下列实验操作或有关叙述正确的是( )
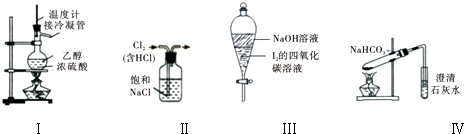

| A、用装置Ⅰ在实验室制备少量乙烯 |
| B、用装置Ⅱ来除去氯气中含有的HCl气体 |
| C、装置Ⅲ中,充分振荡后静置,下层溶液颜色保持不变 |
| D、用装置Ⅳ来探究NaHCO3的热稳定性 |