题目内容
1.用石墨作电极电解3mol•L-1 KCl和0.5mol•L-1 Al2(SO4)3,的混合溶液时,下列电解变化的曲线合理的是( )| A. |  | B. |  | C. |  | D. |  |
分析 Al2(SO4)3水解呈酸性,离子放电顺序为H+>Al3+>Na+,Cl->OH->SO42-,阳极依次发生:2Cl--2e-═Cl2↑,4OH--4e-═O2↑+2H2O;阴极发生2H++2e-=H2↑,结合相关离子的物质的量解答该题.
解答 解:假设混合溶液的体积为1L,
则n(Cl-)=0.3mol,n(Al3+)=0.1mol,
离子放电顺序为H+>Al3+>Na+,Cl->OH->SO42-,
阳极发生:2Cl--2e-═Cl2↑,Cl-离子全部放电,失去0.3mol电子,
阴极反应为2H++2e-═H2↑,得到0.3mol电子,生成0.3molOH-,
发生Al3++3OH-═Al(OH)3↓,
剩余溶液为K2SO4,溶液呈中性,pH=7,
继续电解,为电解水,溶液pH不变,沉淀不溶解.
故选:D.
点评 本题考查电解原理,为高考常见题型,侧重于学生分析能力和计算能力的考查,注意把握离子的放电顺序,难度中等.

练习册系列答案
相关题目
11.下列除去杂质的方法正确的是( )
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液、蒸馏
③除去C2H6中少量的C2H4:气体通过盛有酸性高锰酸钾溶液的洗气瓶
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏.
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液、蒸馏
③除去C2H6中少量的C2H4:气体通过盛有酸性高锰酸钾溶液的洗气瓶
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏.
| A. | ①② | B. | ②④ | C. | ③④ | D. | ②③ |
12.pH相同的氨水和氢氧化钠两种溶液中,它们的( )
| A. | OH-的物质的量相同 | B. | H+ 物质的量浓度相同 | ||
| C. | OH-的物质的量浓度不同 | D. | H+的物质的量浓度不同 |
9.有两个无标签的试剂瓶,分别装有Na2CO3和NaHCO3固体,有四位同学为鉴别它们采用以下不同方法,其中不可行的是( )
| A. | 分别将它们配制成溶液,再加入澄清石灰水 | |
| B. | 分别将它们配制成溶液,再逐滴加入等浓度的稀盐酸 | |
| C. | 分别将它们配制成溶液,再加入CaCl2溶液 | |
| D. | 分别加热,再用石灰水检验是否有CO2产生 |
16. 最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子. N4分子结构如图,已知断裂1mol N-N吸收167kJ热量,生成1molN≡N键放出942kJ热量.根据以上信息和数据,则由N2气体生成1mol气态N4的△H为( )
最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子. N4分子结构如图,已知断裂1mol N-N吸收167kJ热量,生成1molN≡N键放出942kJ热量.根据以上信息和数据,则由N2气体生成1mol气态N4的△H为( )
 最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子. N4分子结构如图,已知断裂1mol N-N吸收167kJ热量,生成1molN≡N键放出942kJ热量.根据以上信息和数据,则由N2气体生成1mol气态N4的△H为( )
最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子. N4分子结构如图,已知断裂1mol N-N吸收167kJ热量,生成1molN≡N键放出942kJ热量.根据以上信息和数据,则由N2气体生成1mol气态N4的△H为( )| A. | +882 kJ/mol | B. | +441 kJ/mol | C. | -882 kJ/mol | D. | -441 kJ/mol |
6. 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与 反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与 反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与 反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与 反应时间(t)的变化示意图如图所示.下列说法不正确的是( )| A. | 反应中转移电子的物质的量是0.21mol | |
| B. | ClO3-的生成可能是由于温度升高引起的 | |
| C. | 苛性钾溶液中KOH的质量是16.8g | |
| D. | 一定有3.36L氯气参加反应 |
13.下列实验的现象与对应结论都正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 灼烧白色粉末,直接观察火焰颜色 | 火焰呈黄色 | 原粉末中有Na+无K+ |
| B | 将一块Al箔在酒精灯火焰上灼烧 | Al箔熔融而不滴落 | Al2O3具有较高的熔点 |
| C | 将一小块Na放入硫酸铜溶液中 | 有铜单质析出 | Na能置换出硫酸铜中的铜 |
| D | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
| A. | A | B. | B | C. | C | D. | D |
10.干冰不能用来扑灭镁条火灾,反应为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,该反应属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
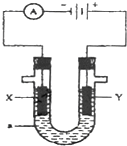 如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: