题目内容
1.欲配制浓度为1.00mol/L的氯化钠溶液100mL,下列用不到的仪器是( )| A. | 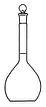 | B. |  | C. |  | D. | 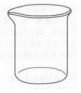 |
分析 用固体配制一定物质的量浓度溶液的一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶,依据各步使用的仪器选择解答.
解答 配制浓度为1.00mol/L的氯化钠溶液100mL,先计算需要氯化钠的质量,然后用托盘天平称量溶质,在烧杯中溶解,用玻璃棒不断搅拌加速固体的溶解,冷却后,用玻璃棒引流入100mL容量瓶,洗涤烧杯和玻璃棒2-3次,并将洗涤液全部转移到容量瓶中,继续加入蒸馏水到离刻度线1-2cm处改用胶头滴管逐滴滴加到凹液面最低处与刻度线相切,然后摇匀,装瓶贴标贴,用到的仪器:托盘天平、烧杯、玻璃棒、药匙、100mL容量瓶、胶头滴管;
用不到分液漏斗;
故选:B.
点评 本题考查了一定物质的量浓度溶液的配制仪器选择,明确配制原理及操作步骤是解题关键,注意容量瓶规格选择,题目难度不大.

练习册系列答案
相关题目
11.将BaO2放入密闭的真空容器中,反应2BaO2(s)?2BaO(s)+O2(g)达到平衡.保持温度不变,体积压缩为原来的一半,体系重新达到平衡,下列说法正确的是( )
| A. | 平衡常数减小 | |
| B. | 平衡逆向移动,氧气的物质的量浓度减小 | |
| C. | 体系的压强不变 | |
| D. | BaO2的量增加 |
12.下列说法正确的是( )
| A. | 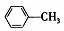 的一溴代物和 的一溴代物和 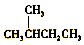 的一溴代物都有4种(不考虑立体异构) 的一溴代物都有4种(不考虑立体异构) | |
| B. | C5H11Cl有3种同分异构体 | |
| C. | 按系统命名法,化合物 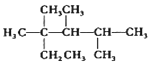 的名称是2,3,4-三甲基-2-乙基戊烷 的名称是2,3,4-三甲基-2-乙基戊烷 | |
| D. | CH3CH═CHCH3分子中的四个碳原子在同一直线上 |
16.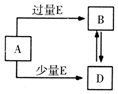 已知A、B、D、E均为中学化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )
已知A、B、D、E均为中学化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )
 已知A、B、D、E均为中学化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )
已知A、B、D、E均为中学化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )| A. | 若A是铁,则E可能为稀硝酸 | |
| B. | 若A是CuO,E是碳,则B为CO | |
| C. | 若A是NaOH溶液,E是CO2,则B为NaHCO3 | |
| D. | 若A是A1C13溶液,E可能是稀氨水 |
6.配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏低的是( )
| A. | NaOH溶解后未经冷却,迅速转移到容量瓶中 | |
| B. | 容量瓶未干燥 | |
| C. | 定容时俯视液面 | |
| D. | 洗涤烧杯和玻璃棒的溶液未转移到容量瓶中 |
13.一定条件下反应N2(g)+3H2(g)?2NH3(g )在10L的密闭容器中进行,测得2min内,N2的物质的量由20mol减小到8mol,则2min内H2的反应速率为( )
| A. | 1.2mol/(L•min) | B. | 1.8 mol/(L•min) | C. | 0.6mol/(L•min) | D. | 2.4mol/(L•min) |
10.下列化学用语使用正确的是( )
| A. | 淀粉的最简式:CH2O | B. | 邻羟基苯甲酸的结构简式: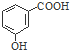 | ||
| C. | 2-乙基-1,3-丁二烯的键线式: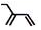 | D. | 苯分子球棍模型: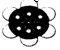 |
14.下表为元素周期表的一部分,请回答下列问题:
(1)③原子结构示意图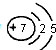 .
.
(2)⑥、⑦和⑧三种元素的最高价氧化物对应水化物酸性最强的是HClO4(填化学式)
(3)①和②元素的最高价氧化物对应水化物碱性最强是中NaOH(填化学式)
(4)⑧元素的单质与①元素的最高价氧化物对应水化物反应的化学方程式:Cl2+2NaOH═NaCl+NaClO+H2O.
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ③ | ④ | ⑤ | |||||
| 3 | ① | ② | ⑥ | ⑦ | ⑧ | |||
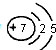 .
.(2)⑥、⑦和⑧三种元素的最高价氧化物对应水化物酸性最强的是HClO4(填化学式)
(3)①和②元素的最高价氧化物对应水化物碱性最强是中NaOH(填化学式)
(4)⑧元素的单质与①元素的最高价氧化物对应水化物反应的化学方程式:Cl2+2NaOH═NaCl+NaClO+H2O.