题目内容
19.下列实验操作能达到相应实验目的是( )| 选项 | 实验操作 | 实验目的 |
| A | 将二氧化硫气体通入紫色石蕊试液中,观察溶液颜色变化 | 证明二氧化硫具有漂白性 |
| B | 验证电离H+的能力HClO>HCO3- | 向 NaHCO3溶液中加入新制氯水,观察溶液中是否有气泡冒出 |
| C | 相同条件下,向两支盛有相同体积不同浓度H2O2溶液的试管中分别滴入适量相同浓度的CuSO4溶液和FeCl3溶液 | 探究Cu2+、Fe3+对H2O2分解速率的影响 |
| D | 向2mL品红溶液和2mL加入少许醋酸的品红溶液中分别滴入3滴84消毒液,观察红色褪色的快慢 | 证明随溶液pH的减少,84消毒液的氧化能力增强 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二氧化硫为酸性氧化物;
B.氯水中含盐酸,盐酸与碳酸氢钠反应;
C.阴离子不同;
D.NaClO具有漂白性,滴有醋酸的品红溶液的红色褪色的快.
解答 解:A.将二氧化硫气体通入紫色石蕊试液中,SO2与水反应产生H2SO3,该物质是酸,具有酸的通性,可以使紫色石蕊试液变为红色,不能证明其漂白性,故A错误;
B.新制氯水中含有稀盐酸,也能使NaHCO3溶液有气泡冒出,不能证明电离H+的能力HClO>HCO3-,故B错误;
C.要探究Cu2+、Fe3+对H2O2分解速率的影响,应该使用的盐的阴离子相同,只有阳离子不同,才可以进行对比,故C错误;
D.向2mL品红溶液和2mL加入少许醋酸的品红溶液中分别滴入3滴NaClO的84消毒液,观察到滴有醋酸的品红溶液的红色褪色的快,说明溶液pH的减少,酸性增强,84消毒液的氧化能力增强,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应、反应速率的影响因素、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度不大.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
7.下列说法中,正确的是( )
| A. | 标准状况下,1mol任何物质的体积都约为22.4L | |
| B. | 1mol任何气体所含分子数都相同,体积也都约为22.4L | |
| C. | 常温常压下,金属Mg从盐酸中置换出1molH2时失去的电子数约1.204×1024 | |
| D. | 同温同压下,相同体积的任何气体单质所含原子数目相同 |
14.下列装置或操作能达到实验目的是( )
| A. |  分离乙酸和乙醇 | B. |  构成锌铜原电池 | C. | 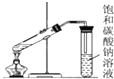 制备乙酸乙酯 | D. | 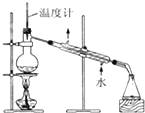 制备蒸馏水 制备蒸馏水 |
4.下列各组溶液只需通过相互滴加就可以鉴别出来的是( )
| A. | NaAlO2溶液和盐酸 | B. | NaHCO3溶液和Ca(OH)2溶液 | ||
| C. | Ba(OH)2溶液和浓MgCl2溶液 | D. | 稀硫酸和碳酸氢钠溶液 |
8.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 在常温常压下,11.2 LN2含有的分子数为0.5 NA | |
| B. | 在常温常压下,1molNe含有的原子数为NA | |
| C. | 71gCl2所含原子数为NA | |
| D. | 在同温、同压下,相同体积的任何气体单质所含的原子数相同 |
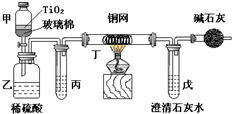 电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.
电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.