题目内容
4.烃A的结构简式为(CH3)2CHCH2CH2C(CH3)3,已知A是由烯烃B跟H2在一定条件下1:1加成制得,则B的结构最多有( )| A. | 6种 | B. | 4种 | C. | 5种 | D. | 3种 |
分析 根据加成反应原理采取逆推法还原C=C双键,烷烃分子中相邻碳原子上均含有氢原子的碳原子间是对应烯烃存在C=C的位置,还原双键时注意重复.
解答 解:根据烯烃与H2加成反应的原理,推知该烷烃分子中相邻碳原子上均含有原子的碳原子间是对应烯烃存在C=C的位置,该烷烃 中能形成双键键位置有:1和2之间、2和3之间、3和4之间,故该烯烃共有3种,故选D.
中能形成双键键位置有:1和2之间、2和3之间、3和4之间,故该烯烃共有3种,故选D.
点评 本题考查了加成反应的运用以及同分异构体的书写,理解加成反应原理是解题的关键,采取逆推法还原C=C双键,注意分析分子结构防止重写、漏写.

练习册系列答案
相关题目
15.表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素是Ar.(用元素符号表示)
(2)②③④三种元素的原子半径从大到小的顺序是Na>Mg>F (用元素符号表示)
(3)用电子式表示③与⑦形成化合物的过程 .
.
(4)在①~⑧元素中,元素的最高价氧化物对应的水化物中碱性最强的NaOH.(填化学式)
(5)在⑦与⑩的单质中,化学性质较活泼的是Cl2(填化学式).
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | VⅡA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)②③④三种元素的原子半径从大到小的顺序是Na>Mg>F (用元素符号表示)
(3)用电子式表示③与⑦形成化合物的过程
 .
.(4)在①~⑧元素中,元素的最高价氧化物对应的水化物中碱性最强的NaOH.(填化学式)
(5)在⑦与⑩的单质中,化学性质较活泼的是Cl2(填化学式).
12.乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明不正确的是( )


| A. | 和金属钠作用时,键①断裂 | |
| B. | 乙醇燃烧时所有键断裂 | |
| C. | 和乙酸、浓硫酸共热制乙酸乙酯时,键②断裂 | |
| D. | 在铜催化下和氧气反应时,键①和③断裂 |
19.下列过程中,共价键被破坏的是( )
| A. | 碘升华 | B. | 干冰汽化 | C. | NaOH熔化 | D. | HCl溶于水 |
9.下列说法正确的是( )
| A. | NaOH固体中只含离子键 | |
| B. | X的气态氢化物的化学式为H2X,则X的最高价氧化物的水化物的化学式为H3XO4 | |
| C. | HCl的形成过程用电子式表示为 | |
| D. | 铝与稀盐酸的反应既是氧化还原反应,又是放热反应 |
16.下列反应中,与其它三个反应不属于同一类型的反应是( )
| A. | 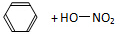 $\underset{\stackrel{浓{H}_{2}S{O}_{4}}{→}}{50~60℃}$ $\underset{\stackrel{浓{H}_{2}S{O}_{4}}{→}}{50~60℃}$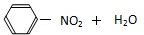 | |
| B. | CH2═CH2+HCl$\stackrel{一定条件}{→}$CH3-CH2Cl | |
| C. | CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O | |
| D. | CH4+Cl2$\stackrel{光照}{?}$CH3Cl+HCl |
13.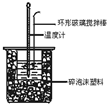 中和热测定实验中,用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验,下列说法不正确的是( )
中和热测定实验中,用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验,下列说法不正确的是( )
 中和热测定实验中,用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验,下列说法不正确的是( )
中和热测定实验中,用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验,下列说法不正确的是( )| A. | 改用60mL 0.50mol/L盐酸跟50mL 0.55 mol/L NaOH溶液进行反应,求出的中和热数值和原来相同 | |
| B. | 用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验比用 50mL0.50mol/L盐酸和50mL0.50mol/LNaOH测得的数值准确 | |
| C. | 酸碱混合时,量筒中NaOH溶液应缓缓倒入小烧杯中,不断用玻璃棒搅拌 | |
| D. | 装置中的大小烧杯之间填满碎泡沫塑料的作用是保温隔热、减少热量损失 |
14.1mol某烃完全燃烧后,生成二氧化碳的体积为89.6L(标准状况),此气态烃在一定条件下能与氢气加成,反应时它与氢气在同温同压下的体积比为1:2,则此烃的结构简式为( )
| A. | CH3-CH═CH2 | B. | CH3-CH2-CH═CH2 | C. |  | D. | CH2═CH-CH═CH2 |
