题目内容
1.下列事故处理措施正确的是( )| A. | 金属钠着火,立即用水灭火 | |
| B. | 在气体发生装置上直接点燃甲烷气体时,必须先检验甲烷的纯度 | |
| C. | 酒精灯不慎着火,应立即吹熄 | |
| D. | 眼睛里溅进盐酸,立即用 NaOH 溶液洗涤眼睛 |
分析 A.钠燃烧生成过氧化钠,过氧化钠、钠都能够与水反应,使火势更加剧烈;
B.可燃性的气体点燃前必须进行验纯;
C.熄灭酒精灯时,不能用嘴吹灭,应该使用灯冒盖灭,否则容易着火;
D.眼里不慎溅入酸碱溶液时,应用大量的水冲洗.
解答 解:A.金属钠着火生成过氧化钠,钠与水反应生成氢气,过氧化钠与水反应生成氧气,所以不能用水灭火,可以用砂子灭火,故A错误;
B.甲烷与空气的混合物比例在一定范围内点燃时会造成爆炸,所以必须验纯,故B正确;
C.酒精灯内有酒精蒸气,用嘴吹灭时,会把火吹入灯内,引起灯内酒精与空气的混合气体爆炸,故C错误;
D.氢氧化钠溶液有较强的腐蚀性,不慎溅入眼中,应用大量水冲洗,故D错误.
故选B.
点评 本题考查了化学实验安全及事故的处理,题目难度不大,明确化学实验基本操作方法为解答关键,注意掌握常见安全事故处理方法,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
相关题目
12.关于粗盐提纯的下列说法中正确的是( )
| A. | 开始析出晶体后用玻璃棒搅拌 | |
| B. | 滤去不溶性杂质后,将滤液移至坩埚内加热浓缩 | |
| C. | 当蒸发到剩余少量液体时,停止加热,利用余热将液体蒸干 | |
| D. | 将制得晶体转移到新制过滤器中用大量水进行洗涤 |
9.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,22.4L辛烷完全燃烧,生成二氧化碳分子数为8NA | |
| B. | 标准状况下,11.2L溴单质含有NA个溴原子 | |
| C. | 常温常压下,28g乙烯和丙烯的混合气体含有的原子总数为6NA | |
| D. | 1mol乙醇与1mol乙酸混合充分反应后生成乙酸乙酯分子数为NA |
16.有八种物质:①甲烷 ②苯 ③聚乙烯 ④1,3-丁二烯 ⑤2-丁炔 ⑥环己烷 ⑦邻二甲苯⑧环己烯,既能使酸性高锰酸钾溶液褪色,又能使溴水因反应而褪色的是( )
| A. | ①④⑤⑧ | B. | ②⑤⑦⑧ | C. | ④⑤⑧ | D. | ③④⑤⑦⑧ |
13.下列化学用语中,正确的是( )
| A. | 过氧化钠的电子式: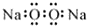 | B. | Cl-离子的结构示意图: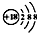 | ||
| C. | 二氧化硅的分子式:SiO2 | D. | HClO的结构式为H-O-Cl |
11.高氯酸是一种酸性极强的无机含氧酸,可用于制备高氯酸盐、人造金刚石提纯等方面.
查阅资料得到以下有关高氯酸的信息:
工业上生产高氯酸的同时还生产了亚氯酸钠,工业流程如图:

(1)操作①的名称是过滤.
(2)反应器Ⅰ中投料时需加入过量浓硫酸,请简述目的为了产物能得到HClO4而不是NaClO4.
(3)反应器Ⅱ中发生反应的离子方程式为4OH-+SO2+2ClO2=2ClO2-+SO42-+2H2O.
(4)某学习小组模拟工业流程图中的蒸馏过程,有液体流出时立即收集产品以获得HClO4纯品.请评价这一操作是否合理并说明理由不合理,因为水的沸点是100℃,HClO4的沸点是130℃,所以最先蒸馏流出的是水而不是HClO4.
(5)若想得到201kg的 HClO4纯品,至少需要NaClO3639kg.
(6)工业上也可用铂作阳极、铜作阴极电解盐酸制得高氯酸,在阳极区可得到20%的高氯酸.写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)4H2O+HCl-8e-=HClO4+8H+.
查阅资料得到以下有关高氯酸的信息:
| 名称 | 分子式 | 外观 | 沸点 |
| 高氯酸 | HClO4 | 无色液体 | 130℃ |

(1)操作①的名称是过滤.
(2)反应器Ⅰ中投料时需加入过量浓硫酸,请简述目的为了产物能得到HClO4而不是NaClO4.
(3)反应器Ⅱ中发生反应的离子方程式为4OH-+SO2+2ClO2=2ClO2-+SO42-+2H2O.
(4)某学习小组模拟工业流程图中的蒸馏过程,有液体流出时立即收集产品以获得HClO4纯品.请评价这一操作是否合理并说明理由不合理,因为水的沸点是100℃,HClO4的沸点是130℃,所以最先蒸馏流出的是水而不是HClO4.
(5)若想得到201kg的 HClO4纯品,至少需要NaClO3639kg.
(6)工业上也可用铂作阳极、铜作阴极电解盐酸制得高氯酸,在阳极区可得到20%的高氯酸.写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)4H2O+HCl-8e-=HClO4+8H+.
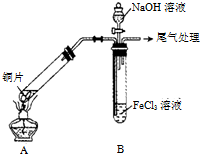 某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示(夹持仪器已略去).
某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示(夹持仪器已略去). 、加聚反应
、加聚反应 、加成反应
、加成反应 、取代反应.
、取代反应.