题目内容
8.在${\;}_{3}^{6}$Li、${\;}_{7}^{14}$N、${\;}_{11}^{23}$Na、${\;}_{12}^{24}$Mg、${\;}_{3}^{7}$Li、${\;}_{6}^{14}$C中,(1)互为同位素的是${\;}_{3}^{6}$Li和${\;}_{3}^{7}$Li;
(2)质量数相等,但不能互称同位素的是${\;}_{7}^{14}$N和${\;}_{6}^{14}$C;
(3)中子数相等,但质子数不相等的是${\;}_{11}^{23}$Na和${\;}_{12}^{24}$Mg.
分析 根据含有相同质子数和不同中子数的原子互称同位素,元素符号的左上角为质量数,以此来判断.
解答 解:(1)${\;}_{3}^{6}$Li;${\;}_{3}^{7}$Li质子数相同中子数不同,互称同位素,故答案为:${\;}_{3}^{6}$Li;${\;}_{3}^{7}$Li;
(2)${\;}_{7}^{14}$N;${\;}_{6}^{14}$C质量数都为14,但质子数不同,不为同位素,故答案为:${\;}_{7}^{14}$N;${\;}_{6}^{14}$C;
(3)${\;}_{11}^{23}$Na、${\;}_{12}^{24}$Mg中子数相等,都为12,但质子数不相等,分别为11,12,故答案为:${\;}_{11}^{23}$Na;${\;}_{12}^{24}$Mg.
点评 本题主要考查了同位素的概念及原子的构成,解答时注意从其概念的要点来分析,难度不大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
11.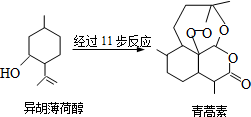 屠呦呦因发明抗疟疾新药青蒿素和双氢青蒿素被授予诺贝尔生理学或医学奖.以异胡薄荷醇为原料是人工合成青蒿素的途径之一(如图).下列说法正确的是( )
屠呦呦因发明抗疟疾新药青蒿素和双氢青蒿素被授予诺贝尔生理学或医学奖.以异胡薄荷醇为原料是人工合成青蒿素的途径之一(如图).下列说法正确的是( )
 屠呦呦因发明抗疟疾新药青蒿素和双氢青蒿素被授予诺贝尔生理学或医学奖.以异胡薄荷醇为原料是人工合成青蒿素的途径之一(如图).下列说法正确的是( )
屠呦呦因发明抗疟疾新药青蒿素和双氢青蒿素被授予诺贝尔生理学或医学奖.以异胡薄荷醇为原料是人工合成青蒿素的途径之一(如图).下列说法正确的是( )| A. | 异胡薄荷醇遇FeCl3溶液显紫色 | |
| B. | 每个青蒿素分子中只含4个六元环 | |
| C. | 异胡薄荷醇可发生消去和加成反应 | |
| D. | 青蒿素在热的酸、碱溶液中均可稳定存在 |
12.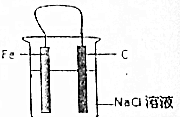 有关Fe-C-Nac1溶液构成的原电池中,叙述错误的是( )
有关Fe-C-Nac1溶液构成的原电池中,叙述错误的是( )
 有关Fe-C-Nac1溶液构成的原电池中,叙述错误的是( )
有关Fe-C-Nac1溶液构成的原电池中,叙述错误的是( )| A. | 铁片为负极,碳棒为正极 | |
| B. | 铁被腐蚀,碳棒上有氯气放出 | |
| C. | 碳棒附近的溶液可使酚酞变红 | |
| D. | 导线上有电流通过,电流方向是由碳极流向铁极 |
9.下列物质中既含有非极性键,又含有极性键的是( )
| A. | CO2 | B. | C2H6 | C. | NaOH | D. | H2O |
3.用NA表示阿伏加德罗常数的值.下列叙述不正确的是( )
| A. | 46g NO2和N2O4以任意比混合,所得混合气体中氧原子数2NA | |
| B. | 标准状况下,含NA个共价键的HF分子所占的体积约为22.4 L | |
| C. | 1mol Fe 与一定量的硝酸反应,转移的电子数为0.2NA~0.3NA | |
| D. | 2mol NO和1mol O2混合,在密闭容器中充分反应后,容器内的分子数小于2NA |
20.分子组成为C9H12的苯的同系物,苯环上只有一个取代基,下列说法正确的是( )
| A. | 该有机物不能发生加成反应,但能发生取代反应 | |
| B. | 该有机物不能使酸性高锰酸钾溶液褪色,但能使溴水褪色 | |
| C. | 该有机物分子中的所有原子可能在同一平面上 | |
| D. | 该有机物的一溴代物最多有11种 |
18.X、Y、Z、T是四种原子序数递增的短周期元素,X形成的简单阳离子核外无电子,Y的最高价氧化物对应的水化物是强酸,Z是人体内含量最多的元素,T在同周期元素形成的简单阳离子中半径最小,则以下说法正确的是( )
| A. | 元素最高化合价的顺序为Z>Y>T>X | |
| B. | Y、Z分别形成的简单氢化物的稳定性为Z>Y | |
| C. | 由X、Y和Z三种元素构成的强电解质,对水的电离均起抑制作用 | |
| D. | 常温下,T的单质与Y的最高价氧化物对应水化物的浓溶液不能反应 |
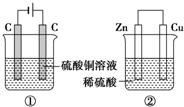 如图两个装置,工作时转移的电子数相等,反应完成后往①中加入19.6gCu(OH)2固体,溶液恰好能恢复到电解前的浓度和体积.若忽略溶液体积的变化,则:
如图两个装置,工作时转移的电子数相等,反应完成后往①中加入19.6gCu(OH)2固体,溶液恰好能恢复到电解前的浓度和体积.若忽略溶液体积的变化,则: