题目内容
设NA为阿伏伽德罗常数的值,下列各项表达中错误的是( )
| A、常温常压下,32g O2和O3的混合气体中含有的原子数为2NA |
| B、标准状况下,33.6L的1H2和3H2均含有3NA个氢原子 |
| C、1mol 131I原子和1mol 123I原子相差4NA个质子 |
D、核外电子分布为 的原子与核外电子排布为 的原子与核外电子排布为 的原子形成1mol化合物时,转移的电子数是NA 的原子形成1mol化合物时,转移的电子数是NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氧气和臭氧分子中都只含有氧原子,根据总质量计算出氧原子的物质的量;
B.根据n=
计算出气体得到物质的量,再计算出含有的氢原子;
C.131I和127I属于同种元素,质子数相等;
D. 为Na原子,
为Na原子, 为Cl原子,二者结合生成NaCl.
为Cl原子,二者结合生成NaCl.
B.根据n=
| V |
| Vm |
C.131I和127I属于同种元素,质子数相等;
D.
 为Na原子,
为Na原子, 为Cl原子,二者结合生成NaCl.
为Cl原子,二者结合生成NaCl.解答:
解:A.氧气和臭氧都是由氧原子构成,32g氧气和臭氧混合物中含O物质的量为:
=2mol,含有的原子总数为2NA,故A正确;
B.标况下3.36L氢气的物质的量为:
=1.5mol,1.5mol氢气气体中含有3mol氢原子,均含有3NA个氢原子,故B正确;
C.1mol123I和131I含有的中子数不同,但是质子数相等,故C错误;
D. 表示Na原子,
表示Na原子, 为Cl原子,二者结合生成1mol氯化钠时转移了1mol电子,转移的电子数是NA,故D正确;
为Cl原子,二者结合生成1mol氯化钠时转移了1mol电子,转移的电子数是NA,故D正确;
故选C.
| 32g |
| 16g/mol |
B.标况下3.36L氢气的物质的量为:
| 3.36L |
| 22.4L/mol |
C.1mol123I和131I含有的中子数不同,但是质子数相等,故C错误;
D.
 表示Na原子,
表示Na原子, 为Cl原子,二者结合生成1mol氯化钠时转移了1mol电子,转移的电子数是NA,故D正确;
为Cl原子,二者结合生成1mol氯化钠时转移了1mol电子,转移的电子数是NA,故D正确;故选C.
点评:本题考查阿伏加德罗常数相关计算和判断,题目难度中等,试题旨在考查考生对化学概念的理解和运用能力,注意熟练掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的关系.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图所示,下列说法正确的是( )
| X | Y |
| Z | W |
| A、若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n为正整数) |
| B、若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱 |
| C、若四种元素均为非金属,则W的最高价氧化物对应的水化物一定是强酸 |
| D、若四种元素只有一种为金厲,则Z、Y 二者的最高价氧化物对应的水化物一定能发生反应 |
化学与生活密切相关,下列说法正确的是( )
| A、明矾可用于水的消毒,杀菌 |
| B、生石灰、铁粉,硅胶是食品包装中常用的干燥剂 |
| C、福尔马林可作食品的保鲜剂 |
| D、二氧化硅可用于制造光导纤维 |
化学与生产、生活、环境密切相关,下列有关说法正确的是( )
| A、半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
| B、“地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
| C、食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质 |
| D、二氧化硫的大量排放是造成光化学烟雾的主要原因 |
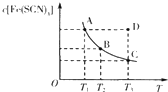 已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )
已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )| A、A点与B点相比,A点的c( Fe3+)大 |
| B、加入KCl固体可以使溶液由D点变到C点 |
| C、反应处于D点时,一定有υ(正)<υ(逆) |
| D、若T1、T2温度下的平衡常数分别为K1、K2,则K1<K2 |
如图为两种途径制备硫酸的过程(反应条件略),下列说法不正确的是( )


| A、途径②增大02浓度可提高SO2转化率 |
| B、含l mol H2S04的浓溶液与足量NaOH反应,放出的热量即为中和热 |
| C、途径②中S02和S03均属于酸性氧化物 |
| D、若△Hl<△H2+△H3,则2H202(aq)=2H20(1)+02 (g)为放热反应 |


 (-R1、-R2-表示氢原子或烃基)
(-R1、-R2-表示氢原子或烃基)
 已知水在25℃和95℃时,其电离平衡曲线如图所示.
已知水在25℃和95℃时,其电离平衡曲线如图所示. 现有W、A、B、C、D、E、F七种前四周期元素,原子序数依次增大.目前公认W、A都各自形成的化合物种类最多.A、B、C位于同周期且第一电离能按A、C、B的顺序依次增大.D、E位于同主族,且D的原子序数为12.F的单质为紫红色常见金属.请回答下列问题:
现有W、A、B、C、D、E、F七种前四周期元素,原子序数依次增大.目前公认W、A都各自形成的化合物种类最多.A、B、C位于同周期且第一电离能按A、C、B的顺序依次增大.D、E位于同主族,且D的原子序数为12.F的单质为紫红色常见金属.请回答下列问题: