题目内容
19.金属冶炼的实质是( )| A. | 金属元素失去电子 | |
| B. | 金属元素获得电子 | |
| C. | 金属元素被氧化了 | |
| D. | 金属元素可能被氧化了,也可能被还原了 |
分析 金属冶炼的实质是金属元素由化合态转变成游离态,金属单质容易失去电子生成化合物,金属冶炼过程就是将高价态金属元素还原为0价,据此分析解答.
解答 解:金属单质容易失去电子生成化合物,金属冶炼实质是金属元素由化合态转变成游离态,过程就是将高价态金属元素对应原子得到电子发生还原反应,还原为0价,
故选:B.
点评 本题考查了金属冶炼的实质,明确氧化还原反应规律及金属存在形态是解题关键,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
9.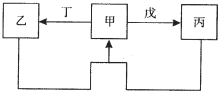 甲、乙、丙、丁、戊五种物质中,甲、乙、丙中均含有某种相同的元素,它们之间具有如图所示转化关系(反应条件及部分产物已略去).下列有关物质的推断不正确的是( )
甲、乙、丙、丁、戊五种物质中,甲、乙、丙中均含有某种相同的元素,它们之间具有如图所示转化关系(反应条件及部分产物已略去).下列有关物质的推断不正确的是( )
 甲、乙、丙、丁、戊五种物质中,甲、乙、丙中均含有某种相同的元素,它们之间具有如图所示转化关系(反应条件及部分产物已略去).下列有关物质的推断不正确的是( )
甲、乙、丙、丁、戊五种物质中,甲、乙、丙中均含有某种相同的元素,它们之间具有如图所示转化关系(反应条件及部分产物已略去).下列有关物质的推断不正确的是( )| 选项 | 假设 | 结论 |
| A | 甲为Al(OH)3 | 丁可能是盐酸 |
| B | 甲为Na2CO3溶液 | 戊可能是CO2 |
| C | 甲为Fe | 丁可能是盐酸 |
| D | 甲为N2 | 戊可能是氧气 |
| A. | A | B. | B | C. | C | D. | D |
10.几种短周期元素的原子半径及某些化合价见下表.分析判断下列说法正确的是( )
| 元素代号 | A | B | D | E | G | I | J | K |
| 化合价 | -1 | -2 | +4 -4 | +7 -1 | +5 -3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
| A. | A的单质是一种常见的还原剂 | |
| B. | A、I、J的离子半径由大到小顺序是A>J>I | |
| C. | G元素的单质不存在同素异形体 | |
| D. | J在DB2中燃烧生成两种化合物 |
7.已知: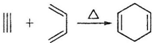 ,如果合成
,如果合成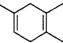 ,所用原始原料可以是( )
,所用原始原料可以是( )
 ,如果合成
,如果合成 ,所用原始原料可以是( )
,所用原始原料可以是( )| A. | 3-甲基-l,3-丁二烯和3-丁炔 | B. | 1,3-戊二烯和2-丁炔 | ||
| C. | 2,3-二甲基-1,3-戊二烯和乙炔 | D. | 2,3-二甲基-l,3-丁二烯和丙炔 |
14.环丙叉环丙烷(A)由于其特殊的电子结构,一直受到结构和理论化学家的注意,由于缺乏有效的合成途径,一度延缓对其反应的研究,直到1993年出现了可以大量制备的方法.根据下列转化,判断下列说法正确的是( )


| A. | A的所有原子都在一个平面内 | B. | 反应①是加成反应 | ||
| C. | 反应②是消去反应 | D. | A的二取代产物只有1种 |
4.某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的元素符号可能是( )
| A. | N | B. | Ne | C. | P | D. | C |
11.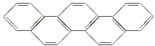 2016年夏季奥运会将在“足球王国”--巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )
2016年夏季奥运会将在“足球王国”--巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )
 2016年夏季奥运会将在“足球王国”--巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )
2016年夏季奥运会将在“足球王国”--巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )| A. | 该有机物属于芳香族化合物,是苯的同系物 | |
| B. | 该有机物中只含非极性键 | |
| C. | 该有机物的一氯代物有11种 | |
| D. | 该有机物完全燃烧生成H2O的物质的量小于CO2的物质的量 |
8.下列离子方程式书写正确的是( )
| A. | AlCl3溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | 用FeCl3溶液刻蚀铜电路板:Cu+Fe3+═Cu2++Fe2+ | |
| C. | 稀硝酸滴到大理石上:CO32-+2H+═H2O+CO2↑ | |
| D. | 铜和浓硝酸反应:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
9.已知I2(aq)+I-(aq)?I3-(aq),下列关于KI溶液的说法不正确的是( )
| A. | 无色的KI溶液在存放过程中会变成黄褐色 | |
| B. | 该溶液中Fe3+、K+、Cl-、H+不能大量共存 | |
| C. | 向碘溶液中加入KI可增大碘的溶解度 | |
| D. | 0.2molKI与Cl2完全反应,消耗的Cl2为2.24L |