题目内容
7.有BaCl2和NaCl的混合溶液a L,将它均分成两份.一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀.反应中消耗x mol H2SO4、y mol AgNO3.据此得知原混合溶液中的Na+的浓度是( )| A. | $\frac{y-2x}{a}$ mol•L-1 | B. | $\frac{y-x}{a}$ mol•L-1 | C. | $\frac{2y-2x}{a}$ mol•L-1 | D. | $\frac{2y-4x}{a}$ mol•L-1 |
分析 由BaCl2和稀硫酸反应可计算Ba2+离子的物质的量,利用NaCl和AgNO3溶液反应计算出Cl-离子的物质的量,由混合液呈电中性可计算出钠离子的物质的量,并注意均分成两份及计算原混合溶液中的c(Na+)来解答即可.
解答 解:设每份中的Ba2+离子的物质的量为m,Cl-离子的物质的量为n,
由Ba2++SO42-═BaSO4↓
1 1
m xmol
得:m=xmol,
Cl-+Ag+═AgCl↓
1 1
n ymol
得:n=ymol,
设每份中的钠离子的物质的量为z,BaCl2和NaCl的混合溶液不显电性,
则x×2+z=y,z=(y-2x)mol,则原溶液中的钠离子为(y-2x)mol×2=(2y-4x)mol,
c(Na+)=$\frac{(2y-4x)mol}{aL}$,故选D.
点评 本题考查学生利用离子反应方程式的计算,明确离子之间的量的关系即可解答,利用溶液不显电性来计算钠离子的物质的量是解答的关键,并注意两等份的关系,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.原子序数为15的元素磷,在周期表中的位置为( )
| A. | 第二周期第ⅤA族 | B. | 第三周期第ⅣA族 | C. | 第三周期第ⅥA族 | D. | 第三周期第ⅤA族 |
15.海水中含有氯化镁,是镁的主要来源之一.从海水中提取镁,可按如下步骤进行:
①把贝壳制成石灰乳;
②在引有海水的水渠中加入石灰乳、沉降、过滤、洗涤沉淀物;
③将沉淀物与盐酸反应,结晶、过滤、干燥产物;
④将得到的产物熔融后电解.
关于提取镁,下列说法正确的是( )
①把贝壳制成石灰乳;
②在引有海水的水渠中加入石灰乳、沉降、过滤、洗涤沉淀物;
③将沉淀物与盐酸反应,结晶、过滤、干燥产物;
④将得到的产物熔融后电解.
关于提取镁,下列说法正确的是( )
| A. | 此法对环境不会造成任何污染 | |
| B. | 沉降、过滤、洗涤沉淀物操作中既有物理变化也有化学变化 | |
| C. | 若提取12 kg Mg,则电子转移1 000 mol | |
| D. | 以上提取镁的过程涉及的离子反应共有3个 |
12.BF3与一定量水形成(H2O)2•BF3晶体Q,Q在一定条件下可转化为R:

晶体Q中各种微粒间的作用力不涉及( )

晶体Q中各种微粒间的作用力不涉及( )
| A. | 离子键 | B. | 共价键 | C. | 配位键 | D. | 氢键 |
19.常春藤皂苷元有刺激黏膜的作用,其结构简式如图.常春藤皂苷元中官能团种类有( )


| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
16.下列有关说法正确的是( )
| A. | 主族元素都属于非金属元素 | |
| B. | 氧元素的相对原子质量为16 | |
| C. | 12C可用于测定古代出土文物的年代 | |
| D. | 氯气通入KI-淀粉溶液中会变蓝 |
19.一个-C3H7和一个-C3H7O取代苯环上的氢原子,形成的有机物中能与金属钠反应的同分异构体有(不考虑立体异构)( )
| A. | 18种 | B. | 24种 | C. | 30种 | D. | 36种 |
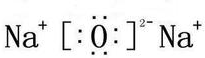 .
.