题目内容
17.A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期.C、B可按原子个数比2:1和1:1分别形成两种离子化合物甲和乙.A原子的最外层电子数比次外层电子数多3个.E是地壳中含量最高的金属元素.根据以上信息回答下列问题:(1)E的元素名称是Al,乙的电子式为
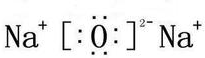 .
.(2)写出甲的化学式Na2O,该化合物中存在的化学键有离子键、共价键
(3)C、D、E三种种元素的离子半径由大到小的顺序是Na+>Mg2+>Al3+ (用离子符号填写).
分析 A、B、C、D、E都是短周期元素,原子序数依次增大,A原子的最外层电子数比次外层电子层多3个,原子只能有2个电子层,最外层电子数为5,故A为N元素;E是地壳中含量最高的金属元素,则E为Al;C、D、E同处另一周期,则C为Na、D为Mg;A、B处于同一周期,C、B可按原子个数比2:1和1:1分别形成两种离子化合物甲和乙,则B为O,甲为Na2O、乙为Na2O2,据此进行解答.
解答 解:A、B、C、D、E都是短周期元素,原子序数依次增大,A原子的最外层电子数比次外层电子层多3个,原子只能有2个电子层,最外层电子数为5,故A为N元素;E是地壳中含量最高的金属元素,则E为Al;C、D、E同处另一周期,则C为Na、D为Mg;A、B处于同一周期,C、B可按原子个数比2:1和1:1分别形成两种离子化合物甲和乙,则B为O,甲为Na2O、乙为Na2O2,
(1)根据分析可知,E为Al元素,名称为铝;乙为过氧化钠,过氧化钠为离子化合物,其电子式为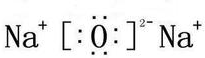 ,
,
故答案为:铝;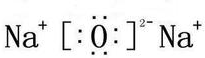 ;
;
(2)甲为氧化钠,其化学式为:Na2O,氧化钠为离子化合物,其化学式中含有离子键和共价键,
故答案为:Na2O;离子键、共价键;
(3)C、D、E位于同一周期,其离子都含有2个电子层,核电荷数越大,离子半径越小,则离子半径大小为:Na+>Mg2+>Al3+,
故答案为:Na+>Mg2+>Al3+.
点评 本题考查了位置、结构与性质关系的关系及应用,题目难度不大,推断元素为解答关键,涉及电子式、化学键、离子半径大小比较等知识,明确原子结构与元素周期律、元素周期表的关系为解答关键,试题培养了学生的灵活应用能力.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
7.2012年6月16日18点37分21秒,神舟九号载人飞船发射成功,与天宫一号目标飞行器进行首次载人空间交会手控对接,使中国的探月工程又迈出重要的一步.据预测,月球的土壤中吸附着数百万吨的氦23He,可作为未来核聚变的重要原料之一.对23He原子的叙述不正确的是( )
| A. | 质量数是3 | B. | 质子数是3 | C. | 中子数是1 | D. | 电子数是2 |
8.目前,消除氮氧化物污染有多种方法.
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4 (g)+4NO2 (g)═4NO(g)+CO2 (g)+2H2 O(g)△H=-574kJ•mol-1
②CH4 (g)+4NO(g)═2N2 (g)+CO2 (g)+2H2 O(g)△H=-1160kJ•mol-1
③H2O(g)═H2O(l)△H=-44.0kJ•mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(1)△H=-955kJ•mol-1.
(2)酸性KMnO4溶液能与草酸(H2C2O4)溶液反应.某探究小组利用反应过程中溶液紫色消失快慢的方法来研究影响反应速率的因素.
Ⅰ.实验前首先用浓度为0.1000mol•L-1酸性KMnO4标准溶液滴定未知浓度的草酸.
①写出滴定过程中发生反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
②滴定过程中操作滴定管的图示正确的是A.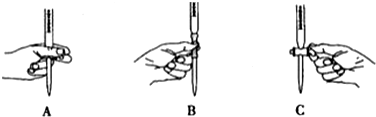
③若配制酸性KMnO4标准溶液时,俯视容量瓶的刻度线,会使测得的草酸溶液浓度偏低(填“偏高”、“偏低”、或“不变”).
Ⅱ.通过滴定实验得到草酸溶液的浓度为0.2000mol•L-1.用该草酸溶液按下表进行后续实验(每次实验草酸溶液的用量均为8mL).
④写出表中a 对应的实验目的探究不同温度对反应速率的影响;
⑤该小组同学对实验1和3分别进行了三次实验,测得以下实验数据(从混合振荡均匀开始计时):
分析上述数据后得出“当其它条件相同时,酸性高锰酸钾溶液的浓度越小,褪色时间就越短,即反应速率就越快”的结论.某同学认为该小组“探究反应物浓度对速率影响”的实验方案设计中存在问题,从而得到了错误的实验结论,请简述改进的实验方案其它条件相同时,利用等量且少量的高锰酸钾与等体积不同浓度的足量草酸溶液反应,测量溶液褪色时间.
⑥该实验中使用的催化剂应选择MnSO4并非MnCl2,原因为(离子方程式表示)为2MnO4-+10Cl-+16H+=5Cl2↑+2Mn2++8H2O.
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4 (g)+4NO2 (g)═4NO(g)+CO2 (g)+2H2 O(g)△H=-574kJ•mol-1
②CH4 (g)+4NO(g)═2N2 (g)+CO2 (g)+2H2 O(g)△H=-1160kJ•mol-1
③H2O(g)═H2O(l)△H=-44.0kJ•mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(1)△H=-955kJ•mol-1.
(2)酸性KMnO4溶液能与草酸(H2C2O4)溶液反应.某探究小组利用反应过程中溶液紫色消失快慢的方法来研究影响反应速率的因素.
Ⅰ.实验前首先用浓度为0.1000mol•L-1酸性KMnO4标准溶液滴定未知浓度的草酸.
①写出滴定过程中发生反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
②滴定过程中操作滴定管的图示正确的是A.

③若配制酸性KMnO4标准溶液时,俯视容量瓶的刻度线,会使测得的草酸溶液浓度偏低(填“偏高”、“偏低”、或“不变”).
Ⅱ.通过滴定实验得到草酸溶液的浓度为0.2000mol•L-1.用该草酸溶液按下表进行后续实验(每次实验草酸溶液的用量均为8mL).
| 实验编号 | 温 度(℃) | 催化剂用量(g) | 酸性高锰酸钾溶液 | 实验目的 a.实验1和2探究 探究不同温度对反应速率的影响 b.实验1 和3 探究反应物浓度对该反应速率的影响; c.实验1 和4 探究催化剂对该反应速率的影 响. | |
| 体积(mL) | 浓度 (mol•L-1) | ||||
| 1 | 25 | 0.5 | 4 | 0.1000 | |
| 2 | 50 | 0.5 | 4 | 0.1000 | |
| 3 | 25 | 0.5 | 4 | 0.0100 | |
| 4 | 25 | 0 | 4 | 0.1000 | |
⑤该小组同学对实验1和3分别进行了三次实验,测得以下实验数据(从混合振荡均匀开始计时):
| 实验编号 | 溶液褪色所需时间(min) | ||
| 第1 次 | 第2 次 | 第3 次 | |
| 1 | 14.0 | 13.0 | 11.0 |
| 3 | 6.5 | 6.7 | 6.8 |
⑥该实验中使用的催化剂应选择MnSO4并非MnCl2,原因为(离子方程式表示)为2MnO4-+10Cl-+16H+=5Cl2↑+2Mn2++8H2O.
5.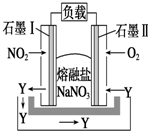 熔融盐NaNO3组成的燃料电池如图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,下列有关说法正确的是( )
熔融盐NaNO3组成的燃料电池如图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,下列有关说法正确的是( )
 熔融盐NaNO3组成的燃料电池如图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,下列有关说法正确的是( )
熔融盐NaNO3组成的燃料电池如图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,下列有关说法正确的是( )| A. | 石墨Ⅰ极为正极,石墨Ⅱ极为负极 | |
| B. | Y的化学式可能为NO | |
| C. | 石墨Ⅰ极的电极反应式为NO2+NO${\;}_{3}^{-}$-e-═N2O5 | |
| D. | 石墨Ⅱ极上发生氧化反应 |
12. 某小组用0.50mol•L-1 NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.
某小组用0.50mol•L-1 NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.
I.配制0.50mol/L NaOH溶液
(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体5.0g.
(2)从如表中选择称量NaOH固体所需要的仪器是(填字母):
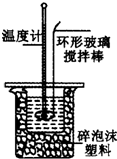
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.
(3)取50mL.NaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
①上表中的温度差平均值为4.0℃;
②近似认为0.50mol/L NaOH溶液和O.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃),则中和热△H-53.5kJ/mol (取小数点后一位).
③上述实验数值结果与57.3kJ•mol叫有偏差,产生偏差的原因可能是acd(填字母).
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.
 某小组用0.50mol•L-1 NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.
某小组用0.50mol•L-1 NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.I.配制0.50mol/L NaOH溶液
(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体5.0g.
(2)从如表中选择称量NaOH固体所需要的仪器是(填字母):
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
(3)取50mL.NaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
| 温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差 平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.6 | |
| 2 | 27.0 | 27.4 | 27.2 | 31.2 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50mol/L NaOH溶液和O.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃),则中和热△H-53.5kJ/mol (取小数点后一位).
③上述实验数值结果与57.3kJ•mol叫有偏差,产生偏差的原因可能是acd(填字母).
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.
9.下列有关有机化合物的性质、结构或用途的说法正确的是( )
| A. | 蛋白质和油脂都属于高分子化合物,一定条件下都能水解 | |
| B. | 乙烯的性质与聚乙烯相同 | |
| C. | 乙醇既可以作燃料,也可以在日常生活中使用,如75%的乙醇经常用于医疗上杀菌、消毒 | |
| D. | 蛋白质溶液中分别加入(NH4)2SO4稀溶液和CuSO4溶液,均有沉淀,原理不相同 |
6.由A、B、C、D四种金属按下表中装置进行实验.
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是A-2e-═A2+.
(2)装置乙,若电路中转移6.02×1022个e-,则C上增加的质量为3.2g.
(3)装置丙中溶液的pH变大(填“变大”“变小”或“不变”).
(4)四种金属活动性由强到弱的顺序是D>A>B>C.
| 装置 | 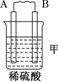 | 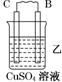 | 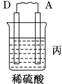 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中负极的电极反应式是A-2e-═A2+.
(2)装置乙,若电路中转移6.02×1022个e-,则C上增加的质量为3.2g.
(3)装置丙中溶液的pH变大(填“变大”“变小”或“不变”).
(4)四种金属活动性由强到弱的顺序是D>A>B>C.
7.有BaCl2和NaCl的混合溶液a L,将它均分成两份.一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀.反应中消耗x mol H2SO4、y mol AgNO3.据此得知原混合溶液中的Na+的浓度是( )
| A. | $\frac{y-2x}{a}$ mol•L-1 | B. | $\frac{y-x}{a}$ mol•L-1 | C. | $\frac{2y-2x}{a}$ mol•L-1 | D. | $\frac{2y-4x}{a}$ mol•L-1 |
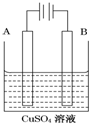 在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置示意图如图.请回答:
在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置示意图如图.请回答: