题目内容
下列表达式错误的是( )
| A、H:Cl | ||
B、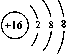 | ||
C、
| ||
| D、O=C=O |
考点:电子式、化学式或化学符号及名称的综合
专题:
分析:A.漏掉了氯原子的3对未成键电子对;
B.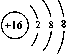 的核电荷数为16、核外电子总数为18,为硫离子;
的核电荷数为16、核外电子总数为18,为硫离子;
C.元素符号的左上角为质量数、左下角为质子数;
D.二氧化碳分子中存在两个碳氧双键,为直线型结构.
B.
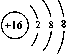 的核电荷数为16、核外电子总数为18,为硫离子;
的核电荷数为16、核外电子总数为18,为硫离子;C.元素符号的左上角为质量数、左下角为质子数;
D.二氧化碳分子中存在两个碳氧双键,为直线型结构.
解答:
解:A.氯化氢为共价化合物,氯原子最外层达到8电子稳定结构,氯化氢正确的电子式为: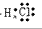 ,故A错误;
,故A错误;
B.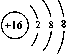 的表示的是硫离子结构示意图,满足离子结构示意图的不是原则,故B正确;
的表示的是硫离子结构示意图,满足离子结构示意图的不是原则,故B正确;
C.188O表示的是质量数为18、质子数为8的氧原子,188O的中子数为:18-8=10,该表示方法合理,故C正确;
D.O=C=O表示的是二氧化碳结构式,符合二氧化碳的结构组成,故D正确;
故选A.
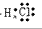 ,故A错误;
,故A错误;B.
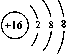 的表示的是硫离子结构示意图,满足离子结构示意图的不是原则,故B正确;
的表示的是硫离子结构示意图,满足离子结构示意图的不是原则,故B正确;C.188O表示的是质量数为18、质子数为8的氧原子,188O的中子数为:18-8=10,该表示方法合理,故C正确;
D.O=C=O表示的是二氧化碳结构式,符合二氧化碳的结构组成,故D正确;
故选A.
点评:本题考查了常见化学用语的表示方法判断,题目难度中等,明确常见化学用语的概念及表示方法为解答关键,注意掌握共价化合物与离子化合物的电子式、离子结构示意图与原子结构示意图的区别,试题有利于培养学生规范答题的能力.

练习册系列答案
相关题目
有Wn+、Xm+、Ym-、Zn-四种离子(m>n),且W、X、Y、Z四种原子的M电子层上的电子数均为奇数.下列说法中正确的是( )
| A、Wn+、Xm+、Ym-、Zn-的离子半径依次增大 |
| B、Y、Z的气态氢化物的热稳定性:YHm>HnZ |
| C、W、X、Y、Z的最高价氧化物对应的水化物都是强电解质 |
| D、W、X、Y、Z的最高价氧化物对应的水化物的碱性依次减弱,酸性依次增强 |
有一系列α-氨基酸按如下特点排列该同系物中所含碳元素的质量分数最大值是( )


| A、32.0% | B、46.6% |
| C、85.7% | D、无法确定 |
2014年我国科学家首次拍摄到水分子团簇的空间取向图象,模型如图.下列关于水的 说法正确的是( )

| A、H2O和D2O是同位素 |
| B、氢氧两种元素只能组成水 |
| C、水分子之间不只存在范德华力 |
| D、图中球棍模型也可表示CO2的结构 |
关于沉淀溶解平衡和溶度积常数,下列说法不正确的是( )
| A、将饱和Na2SO4溶液加入到饱和石灰水中,有白色沉淀产生,说明Ksp[Ca(OH)2]大于Ksp[CaSO4] |
| B、Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 |
| C、已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,该温度下反应Fe(OH)3+3H+?Fe3++3H2O的平衡常数K=4.0×104 |
| D、已知25℃时,Ksp[Mg(OH)2]=1.8×10-11,在MgCl2溶液中加入氨水,测得混合液的pH=11,则溶液中的c(Mg2+)为1.8×10-3mol.L-1 |
 利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如下:
利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如下: