题目内容
关于沉淀溶解平衡和溶度积常数,下列说法不正确的是( )
| A、将饱和Na2SO4溶液加入到饱和石灰水中,有白色沉淀产生,说明Ksp[Ca(OH)2]大于Ksp[CaSO4] |
| B、Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 |
| C、已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,该温度下反应Fe(OH)3+3H+?Fe3++3H2O的平衡常数K=4.0×104 |
| D、已知25℃时,Ksp[Mg(OH)2]=1.8×10-11,在MgCl2溶液中加入氨水,测得混合液的pH=11,则溶液中的c(Mg2+)为1.8×10-3mol.L-1 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:
分析:A、溶度积表达式类型不同,不能说明大小;
B、Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关;
C、依据溶度积常数以及水的离子积常数计算即可;
D、依据pH计算氢离子浓度,然后计算氢氧根浓度,再计算判断即可.
B、Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关;
C、依据溶度积常数以及水的离子积常数计算即可;
D、依据pH计算氢离子浓度,然后计算氢氧根浓度,再计算判断即可.
解答:
解:A.将饱和Na2SO4溶液加入到饱和石灰水中,有白色沉淀产生,说明硫酸钙的溶解度小,但溶度积表达式类型不同,不能说明大小,故A错误;
B.Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关,故B正确;
C.Ksp[Fe(OH)3]=c3(OH-)?c(Fe3+),反应的平衡常数K=
=
=4.0×104故C正确;
D.测得混合液的pH=11,Ksp[Mg(OH)2]=c2(OH-)?c(Mg2+),c(OH-)=10-3,带入求得c(Mg2+)=1.8×10-3mol/L,故D正确;
故选:A.
B.Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关,故B正确;
C.Ksp[Fe(OH)3]=c3(OH-)?c(Fe3+),反应的平衡常数K=
| c(Fe3+) |
| c3(H+) |
| c3(OH-)×c(Fe3+) |
| Kw3 |
D.测得混合液的pH=11,Ksp[Mg(OH)2]=c2(OH-)?c(Mg2+),c(OH-)=10-3,带入求得c(Mg2+)=1.8×10-3mol/L,故D正确;
故选:A.
点评:本题考查了沉淀溶解平衡的应用,溶度积计算分析,平衡移动方向的判断,题目难度中等.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
下列表达式错误的是( )
| A、H:Cl | ||
B、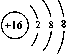 | ||
C、
| ||
| D、O=C=O |
X、Y、Z、M、W五种短周期元素.X的质子总数与电子层数相同,Y、Z、M、W在周期表中的相对位置如下表,且W原子核外电子数是M原子最外层电子数的2倍.下列说法不正确的是( )

| A、原子半径:W>Y>Z>M>X |
| B、X、Y、Z 三种元素形成的化合物中可能既有离子键又有共价键 |
| C、W分别与M、Z元素形成的化合物WM4、WZ2都是原子晶体 |
| D、X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM,沸点X2Z>XM |
一定温度下,在三个体积均为2.0L的恒容密闭容器中发生如下反应:PCl5(g)?PCl3(g)+Cl2(g)
下列说法正确的是( )
| 编号 | 温度(℃) | 起始物质的量 (mol) | 平衡物质的量 (mol) | 达到平衡所需时间 (s) | |
| PCl5(g) | PCl3(g) | Cl2(g) | |||
| Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
| Ⅱ | 320 | 0.80 | t2 | ||
| Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
| A、平衡常数K:容器Ⅱ>容器Ⅲ | ||
| B、反应到达平衡时,PCl5的转化率:容器Ⅱ<容器Ⅰ | ||
C、反应到达平衡时,容器I中的平均速率为v(PCl5)=
| ||
| D、起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl30.45 mol和Cl20.10 mol,则反应将向逆反应方向进行 |
已知25℃时溶解度:AgCl>AgI,若在5mL含有KCl和KI各为0.01mol/L的溶液中,加入8mL 0.01mol/L AgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是( )
| A、c(K+)>c(NO3-)>c(Ag+)=c(Cl-)+c(I-) |
| B、c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) |
| C、c(NO3-)>c(K+)>c(Ag+)>c(Cl-)>c(I-) |
| D、c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-) |
下列图示与对应的叙述相符的是( )
A、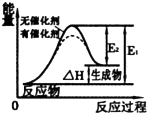 图表示催化剂能改变化学反应的焓变 |
B、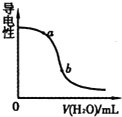 图表示向氨水中加水时溶液导电性的变化情况,且溶液c(OH-)大小:a<b |
C、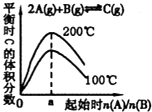 由图可知反应2A(g)+B(g)?C(g)的△H>O,且 a=2 |
D、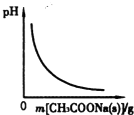 图表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化情况 |
从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是( )
A、 将海带灼烧成灰 |
B、 过滤得含I-溶液 |
C、 萃取后放出碘的CCl4溶液 |
D、 分离碘并回收CCl4 |
