题目内容
 利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如下:
利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如下:根据设计要求回答:
(1)B装置有三种功能:①控制气流速度;②均匀混合气体;③
(2)D装置的石棉中均匀混有KI粉末,其作用是(说明作用并写出反应的方程式)
(3)E装置的作用是
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
(4)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式
(5)E装置除生成盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为
a.CH4 b.CH3Cl c.CH2Cl2 d.CHCl3 e.CCl4.
考点:氯气的实验室制法,甲烷的取代反应
专题:
分析:(1)浓硫酸具有吸水性,能够干燥气体;
(2)氯气氧化性大于碘,能够氧化碘离子生成单质碘;
(3)装置中最后剩余的氯化氢气体需要吸收不能排放到空气中,氯化氢易溶于水需要防止倒吸;
(4)生成的黑色小颗粒为炭黑,光照条件下甲烷和氯气反应生成碳和氯化氢;
(5)最后生成的HCl溶于水生成盐酸,与有机物可用分液的方法分离;一氯甲烷是气体,还可能有过量的甲烷.
(2)氯气氧化性大于碘,能够氧化碘离子生成单质碘;
(3)装置中最后剩余的氯化氢气体需要吸收不能排放到空气中,氯化氢易溶于水需要防止倒吸;
(4)生成的黑色小颗粒为炭黑,光照条件下甲烷和氯气反应生成碳和氯化氢;
(5)最后生成的HCl溶于水生成盐酸,与有机物可用分液的方法分离;一氯甲烷是气体,还可能有过量的甲烷.
解答:
解:(1)浓硫酸具有吸水性,能够干燥气体,所以B装置还能够干燥气体;
故答案为:干燥气体;
(2)氯气氧化性大于碘,能够氧化碘离子生成单质碘,方程式:Cl2+2I-=2Cl-+I2;
故答案为:能吸收过量的氯气,Cl2+2I-=2Cl-+I2;
(3)装置中最后剩余的氯化氢气体需要吸收不能排放到空气中,氯化氢易溶于水需要防止倒吸;
故答案为:CD.
(4)光照条件下甲烷和氯气反应生成碳和氯化氢,反应的方程式:CH4+2Cl2
C+4HCl;
故答案为:CH4+2Cl2
C+4HCl;
(5)E装置中除了有盐酸生成外,还含有二氯甲烷、三氯甲烷和四氯化碳,二氯甲烷、三氯甲烷和四氯化碳不溶于水,能分层,可用分液分开;
反应生成的二氯甲烷、三氯甲烷、四氯化碳均是油状的液体,只有一氯甲烷是气体,还可能有过量的甲烷,
故答案为:分液;ab.
故答案为:干燥气体;
(2)氯气氧化性大于碘,能够氧化碘离子生成单质碘,方程式:Cl2+2I-=2Cl-+I2;
故答案为:能吸收过量的氯气,Cl2+2I-=2Cl-+I2;
(3)装置中最后剩余的氯化氢气体需要吸收不能排放到空气中,氯化氢易溶于水需要防止倒吸;
故答案为:CD.
(4)光照条件下甲烷和氯气反应生成碳和氯化氢,反应的方程式:CH4+2Cl2
| 光照 |
故答案为:CH4+2Cl2
| 光照 |
(5)E装置中除了有盐酸生成外,还含有二氯甲烷、三氯甲烷和四氯化碳,二氯甲烷、三氯甲烷和四氯化碳不溶于水,能分层,可用分液分开;
反应生成的二氯甲烷、三氯甲烷、四氯化碳均是油状的液体,只有一氯甲烷是气体,还可能有过量的甲烷,
故答案为:分液;ab.
点评:本题考查氯气的制备以及甲烷与氯气的取代反应,熟悉氯气的制备原理和性质,熟悉甲烷的取代反应是解题关键,题目难度中等.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
已知反应:①101Kpa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(1);△H=-57.3kJ/mol
下列结论正确的是( )
②稀溶液中,H+(aq)+OH-(aq)=H2O(1);△H=-57.3kJ/mol
下列结论正确的是( )
| A、碳的燃烧热等于110.5 kJ/mol |
| B、①的反应热为221 kJ/mol |
| C、稀硫酸与稀NaOH溶液反应的中和热为57.3kJ/mol |
| D、稀醋酸与稀 NaOH溶液反应生成 1mol水,放出 57.3kJ热量 |
为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列六步操作:
①过滤,②加稍过量的NaOH溶液,③向滤液中加适量盐酸,④加稍过量的Na2CO3溶液,
⑤加稍过量的BaCl2溶液,⑥将滤液蒸发结晶.下列各组操作顺序合理的是( )
①过滤,②加稍过量的NaOH溶液,③向滤液中加适量盐酸,④加稍过量的Na2CO3溶液,
⑤加稍过量的BaCl2溶液,⑥将滤液蒸发结晶.下列各组操作顺序合理的是( )
| A、②④⑤①③⑥ |
| B、⑤②④①③⑥ |
| C、④②⑤①③⑥ |
| D、②⑤④③①⑥ |
物质的量浓度相同的下列溶液中,含离子和分子种类最多的是( )
| A、MgCl2 |
| B、CH3COONa |
| C、氨水 |
| D、K2CO3 |
Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器,其他条件相同时,在Ⅰ、Ⅱ中分别加入3molZ,起始容器的体积均为VL,发生如下反应并达到平衡(X、Y状态未知):aX(?)+2Y(?)?3Z(g),此时Ⅱ中X、Y、Z的物质的量之比为1:2:2,则下列说法一定正确的是( )

| A、若X、Y均为气体,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ |
| B、若X、Y有一种为气体,则平衡时容器的压强:Ⅰ<Ⅱ |
| C、平衡时Ⅱ中Z的转化率为60% |
| D、若X、Y有一种为气体,则平衡是Z的转化率:Ⅰ<Ⅱ |
 下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )| a | b | c | |
| A | Al | AlCl3 | Al(OH)3 |
| B | HNO3 | NO | NO2 |
| C | Si | SiO2 | H2SiO3 |
| D | Na2O | Na2CO3 | NaHCO3 |
| A、A | B、B | C、C | D、D |
下列表达式错误的是( )
| A、H:Cl | ||
B、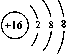 | ||
C、
| ||
| D、O=C=O |
 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.