题目内容
 在温度相同,压强分别为p1、p2条件下,A(g)+2B(g)?nC(g)的反应体系中,C的体积分数(C%)随时间(t)变化的曲线如图所.下列结论正确的是( )
在温度相同,压强分别为p1、p2条件下,A(g)+2B(g)?nC(g)的反应体系中,C的体积分数(C%)随时间(t)变化的曲线如图所.下列结论正确的是( )| A、p1>p2 n<3 |
| B、p1<p2 n>3 |
| C、p1<p2 n=3 |
| D、p1>p2 n>3 |
考点:体积百分含量随温度、压强变化曲线
专题:化学平衡专题
分析:由达到平衡的时间可看出P1>P2,压强增大,C%的百分含量降低,从压强对平衡移动的影响分析.
解答:
解:由达到平衡的时间可看出P2<P1,压强增大,C%的百分含量降低,说明平衡向逆反应方向,则n>3,
故选D.
故选D.
点评:本题考查外界条件对化学平衡移动的影响,题目难度不大,本题注意把握图象的分析,注意从坐标的变化.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A、Na2CO3溶液:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| B、硝酸钠与稀盐酸的混合溶液:c(Na+)=c(NO3-) |
| C、NH4Cl溶液:c(NH4+)=c(Cl-) |
| D、等体积等浓度的氢氧化钠与醋酸混合:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
下列各组离子在溶液中能大量共存,加入氢氧化钠溶液有沉淀生成,加入盐酸有气体生成的一组离子是( )
| A、CO32- Na+ Cu2+ NO3- |
| B、K+ Mg2+ Cl- HCO3- |
| C、NH4+ CO32- NO3- Na+ |
| D、NH4+ Cl- HCO3- K+ |
设NA表示阿伏加德罗常数,数值约为6.02×1023.下列说法正确的是( )
| A、2.4 g金属镁变成镁离子时失去的电子数目为6.02×1022 |
| B、2 g氢气所含分子数目为2×6.02×1023 |
| C、在25℃,1.01×105Pa时,11.2 L氧气所含的氧原子数目为6.02×1023 |
| D、标准状况下,以任意比混合的氢气和氧气混合物2.24 L,所含的分子数为6.02×1022 |
下列化学用语书写正确的是( )
| A、碳酸氢钙CaHCO3 |
B、氯离子的结构示意图为: |
| C、氦气 He2 |
| D、硫酸的电离方程式:H2SO4=H2++SO42- |
等体积、等物质的量浓度的醋酸与氢氧化钠溶液混合,充分反应后,溶液( )
| A、呈中性 | B、呈酸性 |
| C、呈碱性 | D、加紫色石蕊呈红色 |
下列叙述中,正确的是( )
| A、H2SO4的摩尔质量是98g |
| B、将98gH2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2mol/L |
| C、等质量的O2和O3中所含的氧原子数相同 |
| D、标准状况下,1mol任何物质体积均为22.4L |
下列各组离子,在强碱性溶液中可以大量共存的是( )
| A、Cu2+、Ba2+、Cl-、SO42- |
| B、Na+、Ba2+、Cl-、NO3- |
| C、Mg2+、K+、Cl-、NO3- |
| D、Na+、K+、NO3-、H+ |
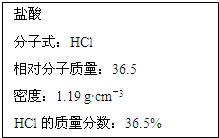 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题: