题目内容
9.(1)写出下列物质在水溶液中的电离方程式:NH3•H2ONH3•H2O?NH4++OH- KAl(SO4)2KAl(SO4)2=K++Al3++2SO42-
(2)写出下列反应的离子方程式
盐酸与醋酸钠CH3COO-+H+=2CH3COOH 碳酸钙与盐酸:CaCO3+2H+═Ca2++H2O+CO2↑
(3)写出下列盐水解的离子方程式:
NH4Cl:NH4++H2O?NH3•H2O+H+ CH3COONa:CH3COO-+H2O?CH3COOH+OH-.
分析 (1)一水合氨为弱电解质,在溶液中部分电离出铵根离子和氢氧根离子;
硫酸铝钾为强电解质,在溶液中完全电离出钾离子、铝离子和硫酸根离子;
(2)醋酸钠与盐酸反应生成醋酸和氯化钠;碳酸钙与盐酸反应生成氯化钙、二氧化碳气体和水;
(3)铵根离子在溶液中部分水解生成一水合氨和氢离子;醋酸根离子结合水电离的氢离子生成弱电解质醋酸.
解答 解:(1)NH3•H2O为弱电解质,部分电离,其电离方程式为:NH3•H2O?NH4++OH-;
KAl(SO4)2在水溶液中完全电离,电离方程式为;KAl(SO4)2=K++Al3++2SO42-,
故答案为:NH3•H2O?NH4++OH-;KAl(SO4)2=K++Al3++2SO42-;
(2)醋酸钠与盐酸反应生成醋酸和氯化钠,反应的离子方程式为:CH3COO-+H+=2CH3COOH;
碳酸钙难溶于水,与盐酸反应生成氯化钙和二氧化碳气体,反应的离子方程式为:CaCO3+2H+═Ca2++H2O+CO2↑,
故答案为:CH3COO-+H+=2CH3COOH;CaCO3+2H+═Ca2++H2O+CO2↑;
(3)氯化铵在溶液中水解生成一水合氨和氯化氢,水解的离子方程式为:NH4++H2O?NH3•H2O+H+;
CH3COONa水解的离子方程式为:CH3COO-+H2O?CH3COOH+OH-,
故答案为:NH4++H2O?NH3•H2O+H+;CH3COO-+H2O?CH3COOH+OH-.
点评 本题考查了水解离子方程式的书写,题目难度中等,水解是可逆的,注意书写水解离子方程式时用可逆号,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.下列各有机物中,属于烃的是( )
| A. | 氯丁烷 | B. | 苯 | C. | 硝基苯 | D. | 甘油 |
17.下列说法中正确的是( )
| A. | 由乙醇制乙烯是放热反应 | |
| B. | 氟氯代烷是一类含氟和含氯的卤代烃 | |
| C. | 木糖醇的结构简式为 ,由此可见它能发生酯化反应,难溶于水 ,由此可见它能发生酯化反应,难溶于水 | |
| D. | 淀粉和纤维素的分子式都是(C6H10O5)n,所以二者是同分异构体 |
4.若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,可能共存的是( )
| A. | NH4+、NO3-、CO32-、Na+ | B. | Na+、Ba2+、HCO3-、[Al(OH)4]- | ||
| C. | NO3-、Ca2+、K+、Fe2+ | D. | NO3-、K+、[Al(OH)4]-、OH- |
14.波尔多液能防治病虫害的原因是( )
| A. | 硫酸铜使菌体蛋白质盐析 | |
| B. | 石灰乳使菌体蛋白质水解 | |
| C. | 铜离子在碱性条件下使菌体蛋白质变性 | |
| D. | 蛋白质可以溶解波尔多液 |
1.不能用离子方程式:CO32-+2H+═CO2↑+H2O来表示的是( )
| A. | 碳酸钠与硫酸氢钠反应 | B. | 碳酸钾溶液与稀盐酸反应 | ||
| C. | 苏打溶液与稀硝酸反应 | D. | 小苏打溶液与稀硫酸反应 |
18.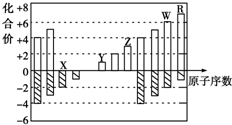 如下图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )
如下图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )
 如下图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )
如下图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )| A. | 气态氢化物的稳定性:R>W | |
| B. | X与Y可以形成原子个数比为1:1和1:2的两种离子化合物 | |
| C. | 由X、Y、Z、W、R五种元素形成的简单离子中半径最小的是X2- | |
| D. | Y和Z两者最高价氧化物对应的水化物能相互反应 |
19.下列叙述正确的是( )
| A. | NH3、CO、CO2都是极性分子 | |
| B. | 10Be、9Be、8Be是摩尔质量不同的三种同素异形体 | |
| C. | HF、HCl、HBr、HI的稳定性依次增强 | |
| D. | HF、HCl、HBr、HI的酸性依次增强 |