题目内容
18.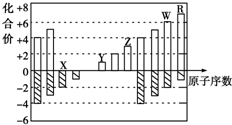 如下图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )
如下图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )| A. | 气态氢化物的稳定性:R>W | |
| B. | X与Y可以形成原子个数比为1:1和1:2的两种离子化合物 | |
| C. | 由X、Y、Z、W、R五种元素形成的简单离子中半径最小的是X2- | |
| D. | Y和Z两者最高价氧化物对应的水化物能相互反应 |
分析 为短周期元素,有两种元素既有+4价,又有-4价,故前一种元素为碳,后一种元素为硅,故R为Si元素,X的化合价为-2价,没有正化合价,故X为O元素,Y的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Y为Na元素,Z为+3价,为Al元素,W的化合价为+6、-2价,故W为S元素,则R为Cl.
解答 解:为短周期元素,有两种元素既有+4价,又有-4价,故前一种元素为碳,后一种元素为硅,故R为Si元素,X的化合价为-2价,没有正化合价,故X为O元素,Y的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Y为Na元素,Z为+3价,为Al元素,W的化合价为+6、-2价,故W为S元素,则R为Cl.
A.非金属性R(Cl)>W(S),故HCl的稳定性比H2S强,故A正确;
B.X与Y可以形成a2O、Na2O2,故B正确;
C.电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,故离子半径:S2->Cl->O2->Na+>Al3+,故C错误;
D.Y和Z两者最高价氧化物对应的水化物分别为NaOH、Al(OH)3,二者发生反应:NaOH+Al(OH)3=NaAlO2+2H2O,故D正确;
故选C.
点评 本题考查结构性质与位置关系、元素周期律等,难度不大,根据推断元素是解题的关键,根据化合价结合原子序数进行推断,首先审题中要抓住“短周期元素”几个字.

练习册系列答案
相关题目
6.下列说法不正确的是( )
| A. | 分子式为C3H8O的有机物不一定是醇 | |
| B. | 乙烯与溴发生加成反应生成1,2-二溴乙烷 | |
| C. | 蛋白质、葡萄糖、脂肪在一定条件下都能发生水解反应 | |
| D. | 用乙醇和浓H2SO4 制备乙烯时,温度计的水银球应浸没于液面下 |
13.短周期元素R、W、X、Y、Z的原子序数依次增大,R原子的最外层电子数是其内层电子数的2倍,X 元素的焰色反应呈黄色,W元素和Z元素同主族,且Z元素的核电荷数是W的2倍,Y是地壳中除氧外含量最多的非金属元素.下列说法不正确的是( )
| A. | W与X形成的两种化合物中阴、阳离子的个数比均为1:2 | |
| B. | Y、R、Z最高价氧化物对应水化物的酸性强弱顺序:Z>R>Y | |
| C. | W的简单氢化物稳定性比Z的简单氢化物稳定性低 | |
| D. | Y与W形成的化合物YW2的熔点高、硬度大 |
3.有8种物质:①甲烷,②丙烯,③1,3丁二烯,④聚乙烯,⑤丙炔,⑥环己烷,⑦邻二甲苯,⑧环己烯(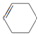 ).其中既能使酸性KMnO4溶液褪色,又能与溴水反应使溴水褪色的是( )
).其中既能使酸性KMnO4溶液褪色,又能与溴水反应使溴水褪色的是( )
 ).其中既能使酸性KMnO4溶液褪色,又能与溴水反应使溴水褪色的是( )
).其中既能使酸性KMnO4溶液褪色,又能与溴水反应使溴水褪色的是( )| A. | ②④⑤⑧ | B. | ②③⑤⑧ | C. | ②④⑤⑦ | D. | ②④⑤⑦⑧ |
7.A、B两种元素,A的原子序数为a,A和B所在周期所含的元素种类分别是m和n,如果A和B同在ⅣA族,当B在A的下一周期时,B的原子序数为( )
| A. | a-n | B. | a+m | C. | a-m | D. | a+n |
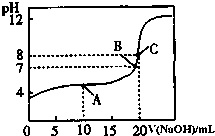 室温下:(1)pH=13的CH3COONa溶液加水稀释100倍后,pH>11(填“>”“=”或“<”);
室温下:(1)pH=13的CH3COONa溶液加水稀释100倍后,pH>11(填“>”“=”或“<”);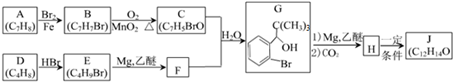
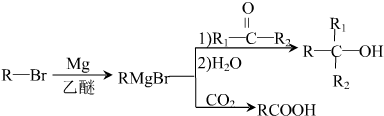
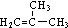 ,D分子中最多有8个原子共平面.
,D分子中最多有8个原子共平面.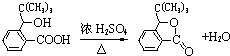 (写明反应条件).
(写明反应条件).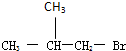 .
.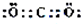 .过量该物质与偏铝酸钠溶液反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.
.过量该物质与偏铝酸钠溶液反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.