题目内容
海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法不正确的是( )
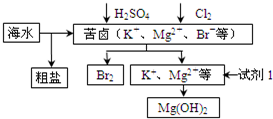

| A、可用BaCl2溶液除去粗盐中的SO42- |
| B、工业上,电解熔融MgO冶炼金属镁 |
| C、试剂1可以选用石灰乳 |
| D、从苦卤中提取Br2的反应的离子方程式为:2Br-+Cl2=2Cl-+Br2 |
考点:海水资源及其综合利用,氯、溴、碘及其化合物的综合应用,金属冶炼的一般原理
专题:化学应用
分析:A.硫酸钡不溶于水和酸;
B.工业上电解熔融氯化镁冶炼镁;
C.石灰乳和镁离子反应生成氢氧化镁沉淀;
D.氯气具有强氧化性,能将溴离子氧化为溴单质.
B.工业上电解熔融氯化镁冶炼镁;
C.石灰乳和镁离子反应生成氢氧化镁沉淀;
D.氯气具有强氧化性,能将溴离子氧化为溴单质.
解答:
解:A.氯化钡和硫酸根离子反应生成难溶性的硫酸钡,且氯离子不是杂质离子,故A正确;
B.氧化镁熔点很高,氯化镁熔点较氧化镁低,电解氧化镁冶炼镁增加成本,所以工业上采用电解熔融氯化镁的方法冶炼镁,故B错误;
C.煅烧贝壳得到CaO,将CaO溶于水得到石灰乳,石灰乳和镁离子反应生成氢氧化镁沉淀,试剂1廉价且原料来源广泛,故C正确;
D.氯气能将溴离子氧化为溴单质,然后采用萃取的方法从溶液中获取溴,故D正确;
故选B.
B.氧化镁熔点很高,氯化镁熔点较氧化镁低,电解氧化镁冶炼镁增加成本,所以工业上采用电解熔融氯化镁的方法冶炼镁,故B错误;
C.煅烧贝壳得到CaO,将CaO溶于水得到石灰乳,石灰乳和镁离子反应生成氢氧化镁沉淀,试剂1廉价且原料来源广泛,故C正确;
D.氯气能将溴离子氧化为溴单质,然后采用萃取的方法从溶液中获取溴,故D正确;
故选B.
点评:本题考查了海水资源的开发和利用,涉及氧化还原反应、除杂、金属的冶炼等知识点,明确物质的性质是解本题关键,知道根据金属活动性强弱选取合适的冶炼方法,题目难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
短周期元素A、B、C的原子序数依次递增,它们的原子最外层电子数之和为10,A和C同主族,B原子的最外层电子数等于A原子次外层电子数.下列叙述中正确的是( )
| A、原子半径:A<B<C |
| B、C的氢化物稳定性大于A的氢化物的稳定性 |
| C、三种元素的最高价氧化物对应的水化物均可由化合反应得到 |
| D、高温下,A单质能转换出C单质 |
用下图表示的一些物质或概念间的从属关系不正确的是( )


| A、X为苯的同系物 Y为芳香烃 Z为芳香族化合物 |
| B、X为离子化合物 Y电解质 Z 化合物 |
| C、X为置换反应 Y氧化还原反应 Z离子反应 |
| D、X为碱性氧化物 Y为金属氧化物 Z为氧化物 |
氮气能大量存在于空气中的根本原因是( )
| A、氮气性质稳定,即使在高温下也很难跟其他物质发生反应 |
| B、氮气比空气轻,且不溶于水 |
| C、氮分子中两个氮原子结合很牢固,分子结构稳定 |
| D、氮气无氧化性,也无还原性,不与其他物质反应 |
小明在做过滤操作时,在老师给他的仪器中,他认为还缺少一种,其中老师给的仪器主要有:漏斗、烧杯、滤纸、铁架台,那么他认为缺少的仪器是( )
| A、小烧杯 | B、玻璃棒 |
| C、药匙 | D、长颈漏斗 |
对于原电池的电极名称,叙述有错误的是( )
| A、发生氧化反应的一极为负极 |
| B、正极为电子流入的一极 |
| C、比较不活泼的金属为负极 |
| D、阳离子移向的一极为正极 |
