题目内容
短周期元素A、B、C的原子序数依次递增,它们的原子最外层电子数之和为10,A和C同主族,B原子的最外层电子数等于A原子次外层电子数.下列叙述中正确的是( )
| A、原子半径:A<B<C |
| B、C的氢化物稳定性大于A的氢化物的稳定性 |
| C、三种元素的最高价氧化物对应的水化物均可由化合反应得到 |
| D、高温下,A单质能转换出C单质 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:短周期元素A、B、C的原子序数依次递增,它们的原子最外层电子数之和为10,A与C同主族,B原子的最外层电子数等于A原子的次外层电子数,则A原子只能有2个电子层,B原子最外层电子数为2,A、C原子最外层电子数=
=4,故A为碳元素、C为Si,结合原子序数可知,B为Mg元素,结合元素周期律与元素化合物性质解答.
| 10-2 |
| 2 |
解答:
解:短周期元素A、B、C的原子序数依次递增,它们的原子最外层电子数之和为10,A与C同主族,B原子的最外层电子数等于A原子的次外层电子数,则A原子只能有2个电子层,B原子最外层电子数为2,A、C原子最外层电子数=
=4,故A为碳元素、C为Si,结合原子序数可知,B为Mg元素,
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径C<Si<Mg,故A错误;
B.A为C元素、C为Si,非金属性C>Si,故A的氢化物稳定性大于C的氢化物稳定性,故B错误;
C.二氧化硅不能与水反应得到硅酸,由可溶性硅酸盐与酸反应得到,故C错误;
D.高温下,碳与二氧化硅反应得到Si与CO,用于生产硅,故D正确.
故选D.
| 10-2 |
| 2 |
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径C<Si<Mg,故A错误;
B.A为C元素、C为Si,非金属性C>Si,故A的氢化物稳定性大于C的氢化物稳定性,故B错误;
C.二氧化硅不能与水反应得到硅酸,由可溶性硅酸盐与酸反应得到,故C错误;
D.高温下,碳与二氧化硅反应得到Si与CO,用于生产硅,故D正确.
故选D.
点评:本题考查结构性质位置关系应用,为高频考点,侧重于学生的分析能力的考查,难度中等,推断元素是解题关键,注意根据B原子最外层电子数特点推断.

练习册系列答案
相关题目
下列说法中不正确的是( )
| A、将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 |
| B、用有机溶剂萃取碘水中的单质碘,所得有机溶液用蒸馏的方法得到固体的碘单质 |
| C、植物油和水的混合溶液可用分液漏斗进行分离 |
| D、分液时,先将下层液体从分液漏斗下口放出,再将上层液体从上口倒出 |
进行过滤操作应选用的一组仪器是( )
| A、玻璃棒、滤纸、烧瓶、漏斗、铁架台 |
| B、滤纸、烧杯、试管夹、漏斗、玻璃棒 |
| C、漏斗、玻璃棒、烧杯、铁架台、滤纸 |
| D、烧杯、酒精灯、试管、铁架台、漏斗 |
某Na2S、Na2SO4、Na2SO3的混合物,测得其中含硫为a%,则含氧为( )
| A、1-a% | ||
B、1-
| ||
C、1-
| ||
| D、无法计算 |
下列说法或表示方法正确的是( )
| A、生成物总能量高于反应物总能量,该反应不能发生 |
| B、需要加热的反应一定是吸热反应 |
| C、由石墨比金刚石稳定,可知C(石墨)(s)═C(金刚石)(s);△H>0 |
| D、稀盐酸和氨水发生中和反应的热化学方程式可表示为:H+(aq)+OH-(aq)═H2O(l);△H=-57.3 kJ?mol-1 |
分离两种互溶的液体且沸点相差较大的实验方法是( )
| A、过滤 | B、蒸馏 | C、分液 | D、萃取 |
下列的叙述中,错误的是( )
| A、油脂属于酯类 |
| B、某些油脂兼有酯和烯烃的一些性质 |
| C、油脂(如植物油)可与H2发生加成反应制得人造脂肪 |
| D、油脂能保持人体的体温,但不能保护内脏器官 |
向某无色溶液中放入铝片,有大量氢气产生,则下列离子在溶液中一定可以大量存在的是( )
| A、CO32- |
| B、SO42- |
| C、HCO3- |
| D、Mg2+ |
海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法不正确的是( )
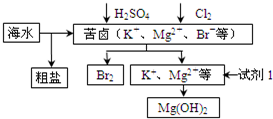

| A、可用BaCl2溶液除去粗盐中的SO42- |
| B、工业上,电解熔融MgO冶炼金属镁 |
| C、试剂1可以选用石灰乳 |
| D、从苦卤中提取Br2的反应的离子方程式为:2Br-+Cl2=2Cl-+Br2 |