题目内容
有关Na2CO3和NaHCO3的比较不正确的是( )
| A、等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,Na2CO3生成的CO2多 |
| B、两者的水溶液都是呈现碱性,可以使无色的酚酞变红色 |
| C、加热时,Na2CO3难分解,但NaHCO3容易分解 |
| D、同温度下,Na2CO3在水中的溶解度比NaHCO3大 |
考点:探究碳酸钠与碳酸氢钠的性质
专题:几种重要的金属及其化合物
分析:A.等质量的Na2CO3和NaHCO3,碳酸钠的摩尔质量大,其物质的量少;
B.碳酸钠和碳酸氢钠在水溶液中均可发生水解,使溶液呈碱性;
C.碳酸氢钠受热易分解,Na2CO3难分解;
D.相同条件下,碳酸氢钠的溶解度小.
B.碳酸钠和碳酸氢钠在水溶液中均可发生水解,使溶液呈碱性;
C.碳酸氢钠受热易分解,Na2CO3难分解;
D.相同条件下,碳酸氢钠的溶解度小.
解答:
解:A.等质量的Na2CO3和NaHCO3,碳酸钠的摩尔质量大,其物质的量少,盐酸足量,则与盐酸完全反应,碳酸钠产生的气体少,故A错误;
B.碳酸钠和碳酸氢钠在水溶液中均可发生水解,使溶液呈碱性,可以使无色的酚酞变红色,故B正确;
C.碳酸氢钠受热易分解,不稳定,则热稳定性为Na2CO3>NaHCO3,故C正确;
D.Na2CO3和NaHCO3在相同条件下,碳酸氢钠的溶解度小,则在水中的溶解度为:Na2CO3>NaHCO3,故D正确;
故选A.
B.碳酸钠和碳酸氢钠在水溶液中均可发生水解,使溶液呈碱性,可以使无色的酚酞变红色,故B正确;
C.碳酸氢钠受热易分解,不稳定,则热稳定性为Na2CO3>NaHCO3,故C正确;
D.Na2CO3和NaHCO3在相同条件下,碳酸氢钠的溶解度小,则在水中的溶解度为:Na2CO3>NaHCO3,故D正确;
故选A.
点评:本题考查碳酸钠和碳酸氢钠的性质,涉及溶解度、稳定性、与酸的反应、水解反应等,注意与酸反应中量少的物质完全反应,题目难度不大.

练习册系列答案
相关题目
 使一镁铝合金粉末在过量稀H2SO4中溶解,在所得溶液中加入NaOH溶液,生成沉淀的质量w和加入NaOH溶液的体积V的关系如图所示,则该合金中镁和铝的质量之比为( )
使一镁铝合金粉末在过量稀H2SO4中溶解,在所得溶液中加入NaOH溶液,生成沉淀的质量w和加入NaOH溶液的体积V的关系如图所示,则该合金中镁和铝的质量之比为( )| A、2:3 | B、1:1 |
| C、4:3 | D、8:9 |
某气体混合物由H2、N2、CO和CH4中的一种或两种组成,将该混合气体点燃后的产物依次通过浓H2SO4和NaOH溶液,结果两溶液的质量均有增加.则该混合气体的组成不可能是( )
| A、N2和CO |
| B、H2和CO |
| C、CH4 |
| D、H2和CH4 |
关于电解CuCl2溶液实验说法正确的是( )
| A、溶液中Cu2+向阳极移动,Cl-向阴极移动 |
| B、阳极上发生还原反应,阴极上发生氧化反应 |
| C、阴极反应:Cu2++2e-=Cu |
| D、可以用湿润的KI淀粉试纸检验阴极产生气体为Cl2 |
下列试剂中,用来检验亚硫酸钠是否被氧化,较为合理的是( )
| A、氯化钡溶液和盐酸 |
| B、硝酸钡溶液和硝酸 |
| C、氢氧化钡溶液和硝酸 |
| D、硝酸钡溶液和盐酸 |
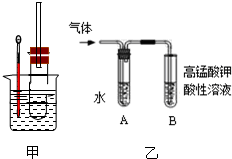 某学习小组用乙醇与氢溴酸为原料制备溴乙烷.该反应发生的原理为:C2H5OH+HBr
某学习小组用乙醇与氢溴酸为原料制备溴乙烷.该反应发生的原理为:C2H5OH+HBr