题目内容
18.化学与生产、生活、社会密切相关.下列有关说法正确的是( )| A. | 福尔马林可用作食品的保鲜剂 | |
| B. | “血液透析”利用了胶体的性质 | |
| C. | 气象环境报告中的“PM2.5”是对一种新分子的描述 | |
| D. | 氢氧化钠可作胃酸的中和剂 |
分析 A.甲醛有毒;
B.血液是胶体;
C.PM2.5是指大气中直径小于或等于2.5微米的颗粒物;
D.氢氧化钠能够中和胃酸中的盐酸,但氢氧化钠具有强烈的腐蚀性.
解答 解:A.甲醛有毒,不能用于食品添加剂,故A错误;
B.血液是胶体,胶粒不能透过半透膜,故B正确;
C.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,不是对一种新分子的描述,故C错误;
D.氢氧化钠的腐蚀性过强,对胃的刺激性过大,不能用于治疗胃酸过多,故D错误.
故选B.
点评 本题考查物质的性质,为高考常见题型,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,提高学习的积极性,注意相关基础知识的积累,难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
6.下列各组物质中,互为同分异构体的是( )
| A. | O2和O3 | B. | ${\;}_{17}^{35}Cl$和${\;}_{17}^{37}Cl$ | ||
| C. | CH3CH2CH2CH3和  | D. | C2H6和C3H8 |
3.设NA为阿伏加罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 LCH4中含有氢原子数目为4NA | |
| B. | 1 molNa2O2中含有的阴离子和阳离子的数目为2NA | |
| C. | 0.1 mol/LCu(NO3)2溶液中含有的离子数目为0.2NA | |
| D. | 28 gN2中所含的原子数目为NA |
7.下列离子方程式书写正确的是( )
| A. | 溴化亚铁溶液中滴加少量氯水:2Br-+Cl2=Br2+2Cl- | |
| B. | NH4HCO3溶液中加入过量氢氧化钠溶液:HCO3-+OH-=CO32-+H2O | |
| C. | NaHSO4溶液中滴加Ba(OH)2溶液至不再产生沉淀:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| D. | 用惰性电极电解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+Cl2↑+H2↑ |

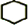 ,名称是环己烷
,名称是环己烷 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$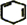 +2NaBr+2H2O.
+2NaBr+2H2O.