题目内容
2.可逆反应A(g)+2B(g)?2C(g)△H<0,在一定条件下达到平衡,若改变条件,将变化情况(增大、减小、不变)填入空格:(1)降低温度,B转化率增大.
(2)使用催化剂,C的物质的量不变.
(3)保持温度和体积不变加入稀有气体,则B的转化率不变.
(4)若温度和体积不变,反应从正反应开始至平衡,在这个变化过程中,容器内气体的密度不变,气体的总物质的量减小.
分析 (1)该反应为放热反应,降低温度,平衡正向移动;
(2)催化剂对平衡移动无影响;
(3)保持温度和体积不变加入稀有气体,A、B、C的浓度不变,平衡不移动;
(4)若温度和体积不变,结合ρ=$\frac{m}{V}$及该反应为气体的物质的量减小的反应来解答.
解答 解:(1)该反应为放热反应,降低温度,平衡正向移动,则B的转化率增大,故答案为:增大;
(2)催化剂对平衡移动无影响,则使用催化剂,C的物质的量不变,故答案为:不变;
(3)保持温度和体积不变加入稀有气体,A、B、C的浓度不变,平衡不移动,则B的转化率不变,故答案为:不变;
(4)若温度和体积不变,气体的m、V不变,由ρ=$\frac{m}{V}$可知密度不变,且该反应为气体的物质的量减小的反应,则反应从正反应开始至平衡,气体的总物质的量减小,
故答案为:不变;减小.
点评 本题考查化学平衡移动及影响因素,为高频考点,把握温度、稀有气体对平衡的影响等为解答的关键,侧重分析与应用能力的考查,注意反应的特点及平衡移动分析,题目难度不大.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
13.下列说法中错误的是( )
| A. | 原子及其离子的核外电子层数等于该元素所在的周期数 | |
| B. | 元素周期表中从IIIB族到IIB族 10个纵行的元素都是金属元素 | |
| C. | 除氦外的稀有气体原子的最外层电子数都是8 | |
| D. | 同一元素的各种同位素的物理性质、化学性质均相同 |
11.下列化学式、电子式、结构式表示正确的是( )
| A. | 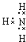 | B. | 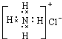 | ||
| C. | 氨水化学式:NH4OH | D. | NH3结构式: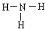 |
12.下列对化学用语的理解正确的是( )
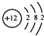
| A. | 原子结构示意图 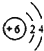 ,可以表示12C原子或13C原子 ,可以表示12C原子或13C原子 | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | 次氯酸的电子式 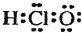 | |
| D. | CO2的比例模型: |
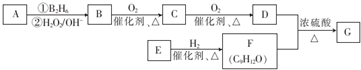
 ;该反应的反应类型为取代反应或酯化反应
;该反应的反应类型为取代反应或酯化反应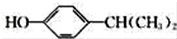 .
.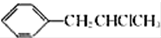 为原料也可合成F,请参考题目中的相关信息写出相应的合成路线图(反应条件中的试剂写在箭头上方,其他写在箭头下方):
为原料也可合成F,请参考题目中的相关信息写出相应的合成路线图(反应条件中的试剂写在箭头上方,其他写在箭头下方):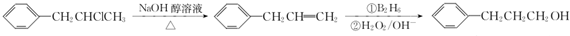 .
.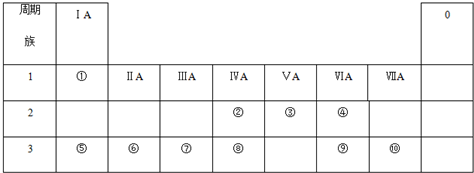
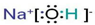
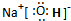 ,所含有的化学键有离子键、极性共价键;它属于离子化合物(填“离子”或“共价”).
,所含有的化学键有离子键、极性共价键;它属于离子化合物(填“离子”或“共价”).