��Ŀ����
15��TiCl4�����������Ѻ��Ѱ�ԭ�ϣ���ҵ����Ҫ��TiO2�Ȼ��ķ�������ȡ��ij��ѧʵ��С����8.0g TiO2������ CCl4Ϊԭ����ȡTiCl4��װ��ͼ1���£�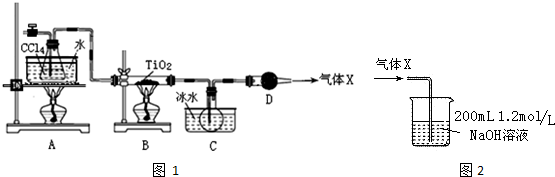
�����й����ʵ����ʣ�
| ���� | �۵�/�� | �е�/�� | ���� |
| CCl4 | -23 | 76.8 | ��TiCl4���� |
| TiCl4 | -25 | 136 | ����ʪ������������ |
��1��TiCl4�л�ѧ���������ǹ��ۼ���
��2��B��TiO2������Ӧ�Ļ�ѧ����ʽ��TiO2��s��+CCl4��g��$\frac{\underline{\;\;��\;\;}}{\;}$TiCl4��g��+CO2��g����
��3��X�������Ҫ�ɷ���CO2��
��4��ʵ�鿪ʼʱ�ȵ�ȼA���ľƾ��ƣ���C����ƿ����Һ�γ���ʱ�ٵ�ȼB���ľƾ��ƣ�����ҪĿ�����ž�ϵͳ��װ�ã��еĿ�����
��5��������Cװ���е�TiCl4��Ӧ���õ�ʵ�����Ϊ������������ƣ���
��6��������Ӧ���������ɵ�����Xȫ��ͨ�뵽ͼ2��ʾ��װ���г�ַ�Ӧ�����ɵ�����Na2CO3���ѧʽ���������ε������ʵ���n��0.1mol��
���� Ϊ��ֹ��ƷTiCl4��������ʵ�鿪ʼʱ�ȵ�ȼA���ľƾ��ƣ�ʹ���Ȼ�̼�ӷ����ž�ϵͳ��װ�ã��еĿ�������C����ƿ����Һ�γ���ʱ�ٵ�ȼB���ľƾ��ƣ�B��װ���ڼ��������£�������ӦTiO2��s��+CCl4��g��$\frac{\underline{\;\;��\;\;}}{\;}$TiCl4��g��+CO2��g����CCl4��TiCl4�۵�ϵͣ�Cװ��ʹ����������ת��ΪҺ̬�������ܻ��ܣ�Ӧ�ò����������룬Dװ�����ӿ���������TiCl4����ʪ������������������ˮ�ⷴӦ����Dװ�������Ƿ�ֹ������ˮ�����룬�ݴ˷������
��� �⣺��1����TiCl4���۷е�ϵͣ���TiCl4Ϊ���Ӿ��壬���ۻ��������TiCl4�л�ѧ���������ǹ��ۼ����ʴ�Ϊ�����ۼ���
��2��TiO2�� CCl4Ϊ�ڼ�������������TiCl4��CO2������Ӧ�ķ���ʽΪ��TiO2��s��+CCl4��g��$\frac{\underline{\;\;��\;\;}}{\;}$TiCl4��g��+CO2��g�����ʴ�Ϊ��TiO2��s��+CCl4��g��$\frac{\underline{\;\;��\;\;}}{\;}$TiCl4��g��+CO2��g����
��3���������Ϸ�����CCl4��TiCl4�۵�ϵͣ�Cװ��ʹ����������ת��ΪҺ̬�������ܻ��ܣ��������ʣ���X������Ҫ��CO2���ʴ�Ϊ��CO2��
��4��Ϊ��ֹ��ƷTiCl4�����������ž�ϵͳ��װ�ã��еĿ���������ʵ�鿪ʼʱ�ȵ�ȼA���ľƾ��ƣ�ʹ���Ȼ�̼�ӷ����ž�ϵͳ��װ�ã��еĿ�������C����ƿ����Һ�γ���ʱ�ٵ�ȼB���ľƾ��ƣ��ʴ�Ϊ���ž�ϵͳ��װ�ã��еĿ�����
��5��CCl4��TiCl4�����ܻ��ܣ�Ӧ�ò����������룬�ʴ�Ϊ������
��6�����ݷ�ӦTiO2��s��+CCl4��g��$\frac{\underline{\;\;��\;\;}}{\;}$TiCl4��g��+CO2��g������8.0g TiO2������ CCl4Ϊԭ����ȡTiCl4��������CO2�����ʵ���Ϊ$\frac{8.0g}{80g/mol}$=0.1mol����200ml1.2mol/L��0.2��1.2=0.24mol��NaOH��Һ��ͨ��0.1molCO2��������Ӧ��2NaOH+CO2�TNa2CO3���������ƹ������������ɵ�����Na2CO3�������ڶ�����̼�ڹ���������ʧ���������ε������ʵ���n��0.1mol��
�ʴ�Ϊ��Na2CO3��0.1mol��
���� ���⿼��ʵ���Ʊ���������ȷԭ���ǽ���ؼ������ؿ���ѧ��װ�õķ������ۣ�ע�����Ŀ��Ϣ����ȡ��Ӧ�ã��Ƕ�ѧ���ۺ������Ŀ��飬��Ŀ�Ѷ��еȣ�

| A�� | ���� | B�� | ���ȼ� | C�� | ������ | D�� | ����� |
| A�� | ��һ��Ԫ����ɵ�����һ���ǵ��� | |
| B�� | �����ܵ����H+�Ļ����ﶼ���� | |
| C�� | ���ܵ����OH-��ʹ��Һ�Լ��ԣ�����Һ�Լ��ԵIJ�һ���Ǽ� | |
| D�� | ������ˮ�γɵ���Һ�ܵ��磬�����ǵ���� |
�����NaCl��NaNO2
1�ⶨ��ҺpH
��pH��ֽ�ֱ�ⶨ0.1mol/L��������Һ��pH�����NaNO2��Һ�ʼ��ԣ�NaNO2��Һ�ʼ��Ե�ԭ����NO2-+H2O?HNO2+OH-�������ӷ���ʽ���ͣ���NaNO2��Һ��c��HNO2��=c��OH-��-c��H+��������Һ���������ӵ�Ũ�ȹ�ϵʽ��ʾ����
2������
ȡ2mL0.1mol/L��������Һ���Թ��У��ֱ�μӼ���ϡ��������Һ����֧�Թܾ�������ɫ�������ֱ�μӼ���ϡ���Ტ��ʢNaNO2��Һ���Թ��г����ܽ⣮���¶��� Ksp��AgNO2��=2��10-8��
Ksp��AgCl��=1.8��10-10��ӦAgNO2��s��+Cl-��aq��?AgCl��s��+NO2-��aq���Ļ�ѧƽ�ⳣ��K=$\frac{1000}{9}$��������д�ɷ�����
������ʵ���ҿ�������װ�ã���ȥ���ּг��������Ʊ��������ƣ�
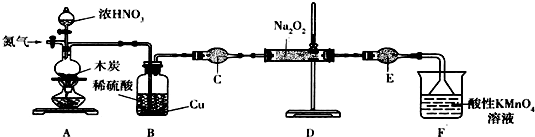
��֪����2NO+Na2O2�T2NaNO2��
�����������£�NO��NO2������MnO4-��Ӧ����NO3-��Mn2+��Na2O2��ʹ���Ը��������Һ��ɫ��
��1������װ��Aǰ����ͨһ��ʱ��N2��Ŀ�����ų�װ���еĿ�����
��2��װ��A�з�����Ӧ�Ļ�ѧ����ʽΪC+4HNO3$\frac{\underline{\;����\;}}{\;}$CO2+4NO2+2H2O��װ��B �������ǽ�NO2 ����ת��ΪNO��Ϊ���淴Ӧ�ṩԭ�ϣ�
��3������C������Ϊ����ܣ�����ʢ�ŵ�ҩƷΪ��ʯ�ң������ƣ���
�������ⶨ�������Ƶĺ���
��ȡ4.000g��ȡ��Ʒ����ˮ���250mL��Һ��ȡ25.00mL��Һ����ƿ�У���0.1000mol•L-1����KMnO4��Һ���еζ���ʵ�������������±���ʾ��
| ������ | ��2 | ��3 | ||
| ��KMnO���/m | ��20.60 | ��20.02 | ��20.00 | ��9.98 |
a����ʽ�ζ���������ˮϴ����δ�ñ�Һ��ϴ
b����ƿϴ����δ����
c���ζ��յ�ʱ���Ӷ���
������KMnO4��Һ�ζ�����������Һ�����ӷ���ʽ6H++2MnO4-+5NO2-=2Mn2++5NO3-+3H2O
�۸��ݱ������ݣ��������ù������������Ƶ���������86.25%�������������λС����
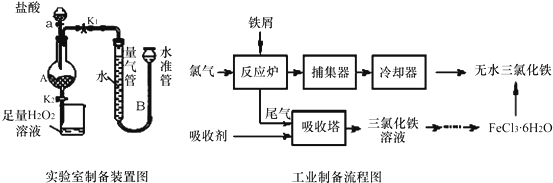
��֪����1����ˮFeCl3���۵�Ϊ555K���е�Ϊ588K��
��2������м�е����ʲ������ᷴӦ
��3����ͬ�¶�����ˮ���Ȼ�����ˮ�е��ܽ�����£�
| �¶�/�� | 0 | 20 | 80 | 100 |
| �ܽ�ȣ�g/100g H2O�� | 74.4 | 91.8 | 525.8 | 535.7 |
���ɼ�K1���رջ���K2��������a�������μ����ᣮ
����ʱ���رյ��ɼ�K1�����ɼ�K2����A����Һ��ȫ�����ձ���رջ���a��
���ձ�����Һ����һϵ�в�����õ�FeCl3•6H2O���壮 ��ش�
��1���ձ���������H2O2��Һ�������ǰ���������ȫ�����������������ӣ�
��2��Ϊ�˲ⶨ����м�����������������������С�������������װ��A�в��������ݻ������ܺ�ˮ��Һ�治�䣮
��3����FeCl3��Һ�Ƶ�FeCl3•6H2O����IJ��������ǣ��������� ������Ũ������ȴ�ᾧ ���ˡ�ϴ�ӡ����
��4����д���������з�Ӧ�����ӷ���ʽ��2Fe2++Cl2=2Fe3++2Cl-��
��5���������¶ȳ���673Kʱ��������Է�������Ϊ325�������Ȼ�������ʵķ���ʽ�����ʽ����Cl-35.5��Fe-56��ΪFe2Cl6��
��6��FeCl3����������ͨ�����õ������ⶨ����ȡm g��ˮ�Ȼ�����Ʒ������ϡ���ᣬ���Ƴ�100mL��Һ��ȡ��10.00mL�������Թ�����KI��Һ����ַ�Ӧ���뼸�ε�����Һ������c mol•L-1 Na2S2O3��Һ�ζ�������V mL����֪��I2+2S2O32-�T2I-+S4O62-����
�ٵζ��յ�������ǣ���Һ����ɫ����ɫ���Ұ�����ڲ���ɫ��
����Ʒ���Ȼ�������������$\frac{162.5cV}{m}$%��
 �ں��º��ݵ��ܱ������У�ͨ��lmolN2��3molH2��������Ӧ��N2��g��+3H2��g��$?_{����}^{���¸�ѹ}$ 2NH3��g����
�ں��º��ݵ��ܱ������У�ͨ��lmolN2��3molH2��������Ӧ��N2��g��+3H2��g��$?_{����}^{���¸�ѹ}$ 2NH3��g����