题目内容
1.某有机物的相对分子质量为102.(1)经测定,该有机物含碳、氢、氧三种元素,其中含氢的质量分数为9.8%,分子中氢原子个数为氧原子的5倍.该有机物的分子式是C5H10O2;若该有机物无甲基、无醚键,且能发生银镜反应,则该有机物的官能团的名称羟基、醛基,写出该有机物与新制的氢氧化铜的反应的化学方程式:
 +2Cu(OH)2+NaOH$\stackrel{△}{→}$
+2Cu(OH)2+NaOH$\stackrel{△}{→}$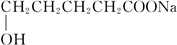 +Cu2O↓+3H2O.
+Cu2O↓+3H2O.(2)经红外光谱测定,该有机物分子中含有一个羧基、一个羟基和一个碳碳双键,则其可能的结构简式为
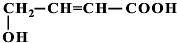 、
、 、
、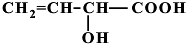 (提示:羟基不能连在碳碳双键上).
(提示:羟基不能连在碳碳双键上).(3)经测定,该有机物只含碳、氢两种元素,且所有原子均在同一平面,请写出该有机物的结构简式:
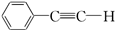 .
.
分析 (1)根据氧元素质量分数计算分子中N(H),进而计算N(O),再根据有机物的相对分子质量计算N(C),据此书写有机物的分子式;若该有机物无甲基、无醚键,且能发生银镜反应,则有机物中含有醛基;
(2)该有机物分子中含有一个羧基(-COOH)、一个羟基(-OH)和一个碳碳双键(C=C),且羟基不能连接在碳碳双键上,此3种官能团的式量为:45+17+24=86,该有机物的相对分子量为102,根据102-86=16可知,该有机物中只能再含有1个C原子,据此判断该有机物可能的结构简式;
(3)根据商余法来确定有机物的分子式,结合分子内所有原子在同一平面内书写其结构简式.
解答 解:(1)有机物分子中N(H)=$\frac{102×9.8%}{1}$=10,
故N(O)=$\frac{10}{5}$=2,
N(C)=$\frac{102-10-16×2}{12}$=5
故该有机物的分子式为C5H10O2,
若该有机物无甲基、无醚键,且能发生银镜反应,则该有机物含有醛基和羟基,结构简式应为 ,在加热条件下与氢氧化铜浊液发生氧化还原反应,方程式为
,在加热条件下与氢氧化铜浊液发生氧化还原反应,方程式为 +2Cu(OH)2+NaOH$\stackrel{△}{→}$
+2Cu(OH)2+NaOH$\stackrel{△}{→}$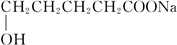 +Cu2O↓+3H2O,
+Cu2O↓+3H2O,
故答案为:C5H10O2;羟基、醛基; +2Cu(OH)2+NaOH$\stackrel{△}{→}$
+2Cu(OH)2+NaOH$\stackrel{△}{→}$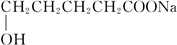 +Cu2O↓+3H2O;
+Cu2O↓+3H2O;
(2)一个羧基(-COOH)、一个羟基(-OH)和一个碳碳双键(C=C)的式量总和为:45+17+24=86,
该有机物的相对分子量为102,根据102-86=16可知,其分子中只能再含有1个C原子,
即:该有机物分子中含有4个C,含有官能团:1个-COOH、1个-OH和1个C=C,可能的结构简式有: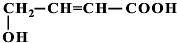 、
、 、
、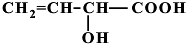 ,
,
故答案为: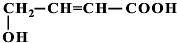 、
、 、
、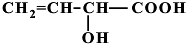 ;
;
(3)因某有机物的相对分子质量为102,且仅含有碳和氢两种元素,根据商余法$\frac{102}{12}$=8…6,由C碳原子与H原子关系可知,分子式为C8H6,不饱和度=$\frac{2×8+2-6}{2}$=6,分子内所有原子在同一平面内,应含有一个苯环、1个C≡C双键,故该有机物结构简式为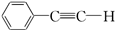 ,故答案为:
,故答案为: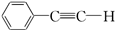 .
.
点评 本题考查了有机物有机物的推断,为高频考点,题目难度中等,注意掌握确定有机物分子式、结构简式的方法,正确理解题干信息为解答本题的关键,试题培养了学生灵活应用所学知识的能力.

 阅读快车系列答案
阅读快车系列答案| A. | 水电离出的c(H+) 减小 | B. | c(OH-) 与 c(H+) 的乘积增大 | ||
| C. | c(H+ ) 减小 | D. | c(OH-) 增大 |
| A. | 次氟酸的结构式为H-F-O | B. | CH4分子的球棍模型: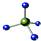 | ||
| C. | 1H、3H2、D互为同位素 | D. | CO2电子式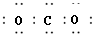 |
| A. | HCl和NH4Cl | B. | CaH2和Na2O2 | C. | NaOH和MgCl2 | D. | H2O2和C2H6 |

| A. | ②、⑧、⑨对应简单离子半径依次减小 | |
| B. | ⑤的三种核素化学性质不同 | |
| C. | 元素=10 ⑩处于常见周期表第四周期第VIIIB族 | |
| D. | ④的最高价氧化物对应的水化物能与其氢化物反应,生成离子化合物 |
①A、B用导线相连后,同时浸入稀H2SO4中,A极为负极;
②C、D用导线相连后,同时浸入稀H2SO4中,电流由D→导线→C;
③A、C用导线相连后,同时浸入稀H2SO4中,C极产生大量气泡;
④B、D用导线相连后,同时浸入稀H2SO4中,D极发生氧化反应.
据此判断四种金属的活动性顺序是( )
| A. | A>B>C>D | B. | C>A>B>D | C. | A>C>D>B | D. | B>D>C>A |
| A. | 分子组成上相差一个或若干个CH2原子团的有机物一定是同系物 | |
| B. | 具有相同的通式且相差一个或若干个CH2原子团的有机物一定是同系物 | |
| C. | 互为同系物的有机物分子结构必然相似 | |
| D. | 互为同系物的有机物通式不一定相同 |
 ,F
,F ,AB2
,AB2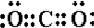 ,A的最简单气态氢化物
,A的最简单气态氢化物 .
.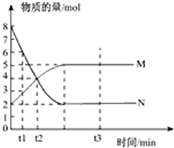 一定温度下,在容积为1L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:
一定温度下,在容积为1L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示: