题目内容
将足量镁条投入到硫酸和硫酸铜的混合溶液中,充分反应后,镁条质量不变.则原溶液中硫酸与硫酸铜的物质的量浓度之比为( )
| A、10:3 | B、5:3 |
| C、1:4 | D、1:1 |
考点:化学方程式的有关计算
专题:计算题
分析:发生反应:Mg+CuSO4=MgSO4+Cu,Mg+H2SO4=MgSO4+H2↑,充分反应后,镁条质量不变,说明Mg与硫酸铜溶液反应固体增重等于与硫酸反应的Mg的质量,令与硫酸反应Mg的质量为24g,根据方程式计算溶液中硫酸、硫酸铜的物质的量,进而计算浓度之比.
解答:
解:充分反应后,镁条质量不变,说明Mg与硫酸铜溶液反应固体增重等于与硫酸反应的Mg的质量,
令与硫酸反应Mg的质量为24g,则:
Mg+CuSO4=MgSO4+Cu 固体增重
1mol 64g-24g=40g
n(CuSO4) 24g
所以n(CuSO4)=
=0.6mol
Mg+H2SO4=MgSO4+H2↑
24g 1mol
故原溶液中硫酸与硫酸铜的物质的量浓度之比=1mol:0.6mol=5:3,
故选B.
令与硫酸反应Mg的质量为24g,则:
Mg+CuSO4=MgSO4+Cu 固体增重
1mol 64g-24g=40g
n(CuSO4) 24g
所以n(CuSO4)=
| 1mol×24g |
| 40g |
Mg+H2SO4=MgSO4+H2↑
24g 1mol
故原溶液中硫酸与硫酸铜的物质的量浓度之比=1mol:0.6mol=5:3,
故选B.
点评:本题考查混合物计算、化学方程式计算,难度中等,关键明确Mg与硫酸铜溶液反应固体增重等于与硫酸反应的Mg的质量,再利用固体质量差量法进行计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在一定条件下体积不变的密闭容器中,一定量的混合气体发生反应:aA(g)+bB(g)?cC(g)△H<0,达到平衡时,测得c(B)=0.48mol?L-1.保持温度不变,把容器体积扩大到原来的2倍,使其重新达到平衡,测得c(B)=0.27mol?L-1.下列有关说法不正确的是( )
| A、a+b>c |
| B、A的转化率增大 |
| C、C的体积分数降低 |
| D、平衡一定逆向移动 |
下列叙述与盐类水解无关的是( )
| A、热纯碱溶液去污能力强 |
| B、明矾可作净水剂 |
| C、Al3+和HCO3-在溶液中不能大量共存 |
| D、配FeCl2溶液加铁粉 |
在甲、乙两个密闭容器中,分别充入HI、NO2,发生反应:(甲)2HI(g)?H2(g)+I2(g)△H>0,(乙)2NO2(g)?N2O4(g)△H<0.下列措施能使两个容器中混合气体颜色均加深且平衡发生移动的是( )
| A、增大反应物浓度 |
| B、增大压强(减小体积) |
| C、降温 |
| D、加催化剂 |
2012年3月22日是第二十届“世界水日”,3月22-28日是第二十五届“中国水周”. 联合国确定今年“世界水日”的宣传主题是“水与粮食安全”( Water and Food Security).下列跟水有关的变化中没有化学变化的是( )
| A、海水晒盐 |
| B、太阳能光解水制氢气 |
| C、饮用水生产 |
| D、肥皂水区分硬水和软水 |
“神舟”五号载人飞船发射成功后,我国又在启动“嫦娥工程”,在3-4年内中国人登上月球.人类探测月球发现,其土壤中存在较丰富的质量数为3的氦,它可以作为核聚变的重要原料之一.以下叙述正确的是( )
| A、由质量数为3的氦原子构成的分子是双原子分子 |
| B、23He与24He的性质均相同 |
| C、23He中的质子数与24He的中子数相等 |
| D、23He、24He 形成的分子中存在共价键 |
下列溶液与铝不能发生反应产生氢气的是( )
| A、盐酸溶液 |
| B、氢氧化钠溶液 |
| C、氯化铵溶液 |
| D、硫酸钠溶液 |
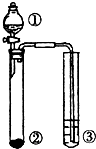 利用图示实验装置,能达到实验目标的是( )
利用图示实验装置,能达到实验目标的是( )