题目内容
下列实验能达到目的是( )
| A、用湿润的碘化钾淀粉试纸鉴别Br2(g)和NO2 |
| B、用稀硫酸和锌粒反应制氢气时加入少许硫酸铜以加快反应速率 |
| C、用量筒量取10.00mL 1.00mol?L-1盐酸于100mL容量瓶中,加水稀释至刻度,可配制0.100 mol?L-1盐酸 |
| D、除去乙酸乙酯中混有的少量乙酸:加入NaOH溶液并加热,振荡、静置后分液 |
考点:化学实验方案的评价,物质的分离、提纯和除杂,物质的检验和鉴别的实验方案设计,配制一定物质的量浓度的溶液
专题:实验评价题
分析:A.NO2和Br2蒸气均有氧化性;
B.利用原电池来分析加快反应速率;
C.量筒量取溶液的体积数值是小数点后一位;
D.乙酸乙酯在氢氧化钠溶液中水解.
B.利用原电池来分析加快反应速率;
C.量筒量取溶液的体积数值是小数点后一位;
D.乙酸乙酯在氢氧化钠溶液中水解.
解答:
解:A.NO2和Br2蒸气均能氧化KI中的碘离子生成碘单质,遇淀粉变蓝,现象相同,不能鉴别,故A错误;
B.加入少许硫酸铜,锌置换出铜,构成锌、铜原电池,从而加快了生成氢气的反应速率,故B正确;
C.量筒量取溶液的体积数值是小数点后一位,所以不能用量筒量取10.00mL盐酸,故C错误;
D.乙酸乙酯在氢氧化钠溶液中水解,应加饱和碳酸钠溶液除杂,故D错误.
故选B.
B.加入少许硫酸铜,锌置换出铜,构成锌、铜原电池,从而加快了生成氢气的反应速率,故B正确;
C.量筒量取溶液的体积数值是小数点后一位,所以不能用量筒量取10.00mL盐酸,故C错误;
D.乙酸乙酯在氢氧化钠溶液中水解,应加饱和碳酸钠溶液除杂,故D错误.
故选B.
点评:本题考查物质的鉴别、化学反应速率、仪器使用以及物质的分离、提纯和检验等,侧重于学生的分析能力和实验能力的考查,注意除杂时不能引入新的杂质,更不能影响被提纯物质的性质,难度不大.

练习册系列答案
相关题目
如图为阿司匹林(用T代表)的结构,下列说法不正确的是( )


| A、T可以发生酯化反应 |
| B、T可以与NaOH溶液反应 |
| C、T属于芳香烃类化合物 |
| D、T在酸中水解可以得到CH3COOH |
把70%的硝酸溶液(ρ=1.40g/cm3)加到等体积的水中,则稀释后硝酸溶液中溶质的质量分数为( )
| A、等于35% | B、小于35% |
| C、大于35% | D、无法确定 |
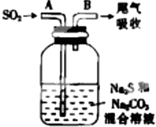 硫、氯及其化合物由广泛的用途.
硫、氯及其化合物由广泛的用途.
