题目内容
10.实验室以正丁醇、溴化钠、硫酸为原料制备正溴丁烷的反应如下:NaBr+H2SO4═HBr+NaHSO4
CH3CH2CH2CH2OH+HBr $\stackrel{△}{→}$ CH3CH2CH2CH2Br+H2O
在圆底烧瓶中加入原料,充分振荡后加入几粒沸石,安装装置Ⅰ.加热至沸腾,反应约40min.待反应液冷却后,改装为装置Ⅱ,蒸出粗产品.部分物理性质列表如下:

| 物质 | 正丁醇 | 正溴丁烷 |
| 沸点/℃ | 117.2 | 101.6 |
| 熔点/℃ | -89.12 | -112.4 |
| 密度/g•cm-3 | 0.8098 | 1.2758 |
| 溶解性 | 微溶于水,溶于浓硫酸 | 不溶于水和浓硫酸 |
回答下列问题:
(1)仪器A的名称是球形冷凝管,冷却水从A的下(填“上”或“下”)口通入.
(2)在圆底烧瓶中加入的原料有:①10ml水;②7.5ml正丁醇;③10g溴化钠;④12mL浓硫酸.上述物质的加入顺序合理的是a(填正确答案标号).
a.①④②③b.④①②③c.③④①②
(3)烧杯B中盛有NaOH溶液,吸收的尾气主要是HBr(填化学式).本实验使用电热套进行加热,总共使用了3次.
(4)用浓硫酸洗涤粗产品时,有机层从分液漏斗上口倒出(填“上口倒出”或“下口放出”).最后一次水洗主要是洗掉有机物中少量的碳酸氢钠.
(5)制备正溴丁烷时,不直接用装置Ⅱ边反应边蒸出产物,其原因是正丁醇、正溴丁烷的沸点相差较小,若边反应边蒸馏,会有较多的正丁醇被蒸出,使产率降低.
(6)本实验得到正溴丁烷6.5g,产率为$\frac{6.5×74}{7.5×0.8098×137}$×100%(只列式,不必计算出结果).
分析 (1)根据装置图可知仪器A名称,冷凝管充满冷凝水充分冷却,逆流冷却效果好;
(2)浓硫酸稀释时,必须将浓硫酸慢慢倒入水中,冷却后加入丁醇,减少挥发,最后加入NaBr;
(3)正丁醇、溴化钠、硫酸反应时,会有挥发出来的溴化氢,用氢氧化钠溶液吸收;实验中在反应生成CH3CH2CH2CH2Br时要加热,装置Ⅱ蒸出粗产品需要加热,粗产品洗涤、分液后分离出有机层,加入无水氯化钙固体后常压蒸馏收集99~103℃馏分,也需要加热;
(4)有机层的密度小于浓硫酸,有机层在上层;最后一次水洗主要是除去有机物中少量的碳酸氢钠;
(5)正丁醇、正溴丁烷的沸点相差较小;
(6)7.5ml正丁醇的物质的量为$\frac{7.5mL×0.8098g/mL}{74g/mol}$mol=0.082mol,10g溴化钠的物质的量为$\frac{10g}{103g/mol}$mol=0.097mol,根据反应NaBr+H2SO4═HBr+NaHSO4、CH3CH2CH2CH2OH+HBr$\stackrel{△}{→}$CH3CH2CH2CH2Br+H2O可知,是正丁醇不足量,根据正丁醇的质量计算正溴丁烷理论产量,产率=(实际产量÷理论产量)×100%.
解答 解:(1)根据仪器a的结构特征,可知仪器a是球形冷凝管,冷凝管充满冷凝水充分冷却,冷却水从A的下口通入,
故答案为:球形冷凝管;下;
(2)浓硫酸稀释时,必须将浓硫酸慢慢倒入水中,冷却后加入丁醇,减少挥发,最后加入NaBr,
故选:a;
(3)正丁醇、溴化钠、硫酸反应时,会有挥发出来的HBr,用氢氧化钠溶液吸收,实验中在反应生成CH3CH2CH2CH2Br时要加热,装置Ⅱ蒸出粗产品需要加热,粗产品洗涤、分液后分离出有机层,加入无水氯化钙固体后常压蒸馏收集99~103℃馏分,也需要加热,所以共有三次用电热套进行加热,
故答案为:HBr;3;
(4)有机层的密度小于浓硫酸,所以有机层在上层,要从分液漏斗上口倒出,按实验步骤可知,最后一次水洗主要是除去有机物中少量的碳酸氢钠,
故答案为:上口倒出;有机物中少量的碳酸氢钠;
(5)正丁醇、正溴丁烷的沸点相差较小,若边反应边蒸馏,会有较多的正丁醇被蒸出,使产率降低,所以制备正溴丁烷时,不直接用装置Ⅱ边反应边蒸出产物,
故答案为:正丁醇、正溴丁烷的沸点相差较小,若边反应边蒸馏,会有较多的正丁醇被蒸出,使产率降低;
(6)7.5ml正丁醇的物质的量为$\frac{7.5mL×0.8098g/mL}{74g/mol}$mol=0.082mol,10g溴化钠的物质的量为$\frac{10g}{103g/mol}$mol=0.097mol,根据反应NaBr+H2SO4═HBr+NaHSO4、CH3CH2CH2CH2OH+HBr$\stackrel{△}{→}$CH3CH2CH2CH2Br+H2O可知,是正丁醇不足量,则正溴丁烷理论产量为7.5×0.8098×$\frac{137}{74}$g,故产率=[6.6g÷(7.5×0.8098×$\frac{137}{74}$g)]×100%=$\frac{6.5×74}{7.5×0.8098×137}$×100%,
故答案为:$\frac{6.5×74}{7.5×0.8098×137}$×100%.
点评 本题考查有机物的合成实验、基本操作、物质的分离提纯、实验条件的控制与分析评价等,是对学生综合能力的考查,需要学生具备扎实的基础,注意题目数据的运用,难度中等.

| A. | C | B. | Cu | C. | A1 | D. | Fe |
| A. | 第六周期ⅢA族 | B. | 第五周期ⅢA族 | C. | 第六周期ⅢB族 | D. | 第五周期ⅢB族 |
①NH4Cl溶液 ②KOH溶液 ③Na2CO3溶液 ④热的乙醇 ⑤苯
⑥醋酸溶液⑦FeCl3 溶液 ⑧CuSO4 溶液 ⑨NaH2PO4 ⑩NaHCO3 溶液.
| A. | ①⑥⑦⑧ | B. | ③④⑤⑨⑩ | C. | ②③⑤⑩ | D. | ③④⑤⑦ |
| A. | Ca | B. | N | C. | Si | D. | Al |
| 物质 | 氧化镁 | 氯化镁 |
| 熔点/℃ | 2 852 | 714 |
| A. | 海水$\stackrel{NaOH溶液}{→}$Mg(OH)2$\stackrel{通电}{→}$Mg | |
| B. | 海水$\stackrel{盐酸}{→}$MgCl2溶液-→MgCl2(熔融)$\stackrel{通电}{→}$Mg | |
| C. | 海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{盐酸}{→}$MgCl2溶液-→MgCl2(熔融)$\stackrel{通电}{→}$Mg | |
| D. | 海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{灼烧}{→}$MgO$\stackrel{通电}{→}$Mg |
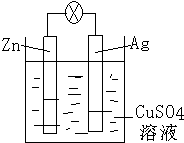 (1)燃料电池是一种高效、环境友好的发电装置.氢氧燃料电池已用于航天飞机.以氢氧化钾溶液为电解质溶液的这种电池的负极反应式为2H2+4OH--4e-═4H2O,这种电池在放电使用一段时间后,电解质溶液中的c(OH-)将减小(填“增大”“减小”或“不变”).
(1)燃料电池是一种高效、环境友好的发电装置.氢氧燃料电池已用于航天飞机.以氢氧化钾溶液为电解质溶液的这种电池的负极反应式为2H2+4OH--4e-═4H2O,这种电池在放电使用一段时间后,电解质溶液中的c(OH-)将减小(填“增大”“减小”或“不变”).