题目内容
2.短周期主族元素X、Y、Z、W原子序数依次增大,X原子最外层有4个电子,Y是地壳中含量最高的元素,Z在周期表中处于周期序数等于族序数的位置,W的单质广泛用作半导体材料.下列叙述正确的是( )| A. | X、Y、Z、W四种元素的最外层电子数之和为18 | |
| B. | 原子半径由大到小的顺序:W>Z>Y>X | |
| C. | 单质的熔点:W>Z | |
| D. | 简单气态氢化物的稳定性:X>Y>W |
分析 短周期主族元素X、Y、Z、W原子序数依次增大,Y是地壳中含量最高的元素,则Y为O元素,结合原子序数及X原子最外层有4个电子,则X为C;Z在周期表中处于周期序数等于族序数的位置,则Z为第三周期第ⅢA族元素Al,W的单质广泛用作半导体材料,则W为Si,然后结合元素周期律及元素化合物知识来解答.
解答 解:短周期主族元素X、Y、Z、W原子序数依次增大,Y是地壳中含量最高的元素,则Y为O元素,结合原子序数及X原子最外层有4个电子,则X为C;Z在周期表中处于周期序数等于族序数的位置,则Z为第三周期第ⅢA族元素Al,W的单质广泛用作半导体材料,则W为Si,
A.X、Y、Z、W四种元素的最外层电子数之和为4+6+3+4=17,故A错误;
B.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径由大到小的顺序:Z>W>C>Y,故B错误;
C.Si为原子晶体,Al为金属晶体,则单质的熔点:W>Z,故C正确;
D.非金属性越强,对应氢化物越稳定,则简单气态氢化物的稳定性:Y>X>W,故D错误;
故选C.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、性质、元素周期律及元素化合物知识为解答的关键,侧重分析与应用能力的考查,注意选项C为解答的难点,题目难度不大.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目
12.如图实验装置图正确的是( )
| A. | 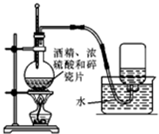 实验室制乙烯 | B. | 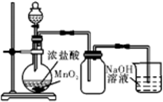 实验室制氯气 | ||
| C. | 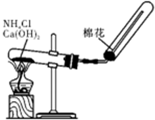 实验室制氨气 | D. |  实验室制乙酸乙酯 |
13.水是人类赖以生存的物质.H2O的摩尔质量的数值是( )
| A. | 16 | B. | 18 | C. | 20 | D. | 22 |
10.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 淀粉溶液中加稀硫酸,加热片剂,滴加银氨溶液,再水浴加热 | 无银镜生成 | 淀粉未发生水解 |
| B | 将一铝箔放在酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面生成致密的Al2O3薄膜,且Al2O3熔点高于Al |
| C | 铜放入稀硫酸中,再加入硝酸钠固体 | 开始无明显现象,后溶液变蓝,有明显的气泡放出,铜溶解 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 向2mL0.1mol/LNa2S溶液中滴加几滴0.1mol/LZnSO4溶液;再加入几滴0.1mol/LCuSO4溶液 | 先生成白色沉淀,后生成黑色沉淀 | 溶度积(Ksp):ZnS>CuS |
| A. | A | B. | B | C. | C | D. | D |
17.下列混合气体和水反应时,一种气体的体积减少,另一种气体的体积增加的是( )
| A. | 二氧化氮和一氧化氮 | B. | 氢气和氧气 | ||
| C. | 氧气和二氧化氮 | D. | 氯气和氧气 |
14.有机物在反应中,常有下列原子间的共价键全部或部分断裂,如C-H、C-C、C═C、C-O、C═O、O-H等.下列各反应中,反应物分子中断裂的键和反应类型对应正确的是( )
| 化学反应 | 加成反应 | 乙酸酯化 | 乙醇酯化 | 乙醇的催化氧化 |
| A | C=C | C-O | O-H | C-H、O-H |
| B | C=C | C-O | O-H | C-O |
| C | C-C | C=O | C-O | C-H |
| D | C=C | C-O | C-O | C-C |
| A. | A | B. | B | C. | C | D. | D |
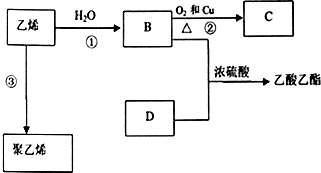 已知乙烯能发生以下转化:
已知乙烯能发生以下转化: .
. 氮及其化合物与人们的生活息息相关,请回答下列有关问题.
氮及其化合物与人们的生活息息相关,请回答下列有关问题.