题目内容
12.如图实验装置图正确的是( )| A. | 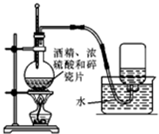 实验室制乙烯 | B. | 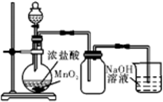 实验室制氯气 | ||
| C. | 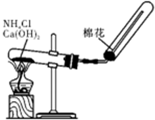 实验室制氨气 | D. |  实验室制乙酸乙酯 |
分析 A.乙醇在170℃发生消去反应生成乙烯;
B.浓盐酸与二氧化锰反应需要加热;
C.氯化铵与氢氧化钙加热生成氨气,氨气的密度比空气密度小;
D.导管在碳酸钠溶液的液面下,易发生倒吸.
解答 解:A.乙醇在170℃发生消去反应生成乙烯,则图中温度计的水银球没有在液面下,故A错误;
B.浓盐酸与二氧化锰反应需要加热,则图中缺少加热装置,故B错误;
C.氯化铵与氢氧化钙加热生成氨气,氨气的密度比空气密度小,则图中反应及收集装置均合理,故C正确;
D.导管在碳酸钠溶液的液面下,易发生倒吸,则图导管应在碳酸钠溶液的液面上,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、物质的制备实验等为解答的关键,侧重分析与实验能力的考查,注意反应原理及实验评价性分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列实验操作,不能用以分离提纯物质的是( )
| A. | 萃取 | B. | 称量 | C. | 蒸馏 | D. | 蒸发 |
20.在一定条件下的定容密闭容器中,下列说法能表明反应A(s)+2B(g)═C(g)+D(g) 已达平衡状态的是( )
| A. | 混合气体的压强不再改变 | |
| B. | 单位时间内生成nmolA的同时,生成2nmol的B | |
| C. | C的生成速率是B的生成速率的两倍 | |
| D. | 混合气体的密度不再改变 |
7.下列离子在溶液中因发生氧化还原反应而不能大量共存的是( )
| A. | H+、Na+、Cl- | B. | H+、Ag+、Cl- | C. | Na+、H+、NO3- | D. | Fe2+、H+、NO3- |
17.甲烷分子是以碳原子为中心的正四面体结构,而不是正方形的平面结构,理由是( )
| A. | CH3Cl只有一种结构 | B. | CH2Cl2只有一种结构 | ||
| C. | CHCl3只有一种结构 | D. | CH4中含有4个C-H极性键 |
1.化学与生活.社会密切相关,下列说法不正确的是( )
| A. | 提倡人们购物时减少使用塑料袋,是为了减少白色污染 | |
| B. | 绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染 | |
| C. | 为防止电池中的重金属等污染土壤和水体,应进行集中填埋处理 | |
| D. | 硫氧化物和氮氧化物是形成酸雨的主要物质 |
2.短周期主族元素X、Y、Z、W原子序数依次增大,X原子最外层有4个电子,Y是地壳中含量最高的元素,Z在周期表中处于周期序数等于族序数的位置,W的单质广泛用作半导体材料.下列叙述正确的是( )
| A. | X、Y、Z、W四种元素的最外层电子数之和为18 | |
| B. | 原子半径由大到小的顺序:W>Z>Y>X | |
| C. | 单质的熔点:W>Z | |
| D. | 简单气态氢化物的稳定性:X>Y>W |
