题目内容
16.下列指定反应的离子方程式正确的是( )| A. | 用FeCl3溶液腐蚀铜板:Fe3++Cu═Fe2++Cu2+ | |
| B. | 向氨水中通入过量SO2:SO2+2NH3•H2O═2NH4++SO32-+H2O | |
| C. | 用MnO2与浓盐酸反应制Cl2:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O | |
| D. | 在强碱性溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3+4OH-═2FeO43-+3Cl-+5H2O |
分析 A.电荷不守恒;
B.二氧化硫过量,反应生成亚硫酸氢铵;
C.氯化氢为强电解质,应拆成离子形式;
D.二者发生氧化还原反应生成高铁酸根子和氯离子、水.
解答 解:A.用FeCl3溶液腐蚀铜板,离子方程式:2Fe3++Cu═2Fe2++Cu2+,故A错误;
B.将过量SO2气体通入氨水中,反应生成亚硫酸氢铵,反应的离子方程式为:SO2+NH3•H2O=NH4++HSO3-,故B错误;
C.用MnO2与浓盐酸反应制Cl2,离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,故C错误;
D.在强碱性溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4,离子方程式:3ClO-+2Fe(OH)3+4OH-═2FeO43-+3Cl-+5H2O,故D正确;
故选:D.
点评 本题考查了离子方程式的书写判断,题目难度中等,注意离子反应遵循客观事实、遵循原子个数、电荷守恒规律,注意化学式的拆分,充分考查了学生的分析、理解能力及灵活应用能力.

练习册系列答案
 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
6.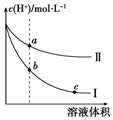 某温度下,等体积、c(H+)相同的盐酸和醋酸溶液分别加水稀释,溶液中的c(H+)随溶液体积变化的曲线如图所示.据图判断下列说法正确的是( )
某温度下,等体积、c(H+)相同的盐酸和醋酸溶液分别加水稀释,溶液中的c(H+)随溶液体积变化的曲线如图所示.据图判断下列说法正确的是( )
 某温度下,等体积、c(H+)相同的盐酸和醋酸溶液分别加水稀释,溶液中的c(H+)随溶液体积变化的曲线如图所示.据图判断下列说法正确的是( )
某温度下,等体积、c(H+)相同的盐酸和醋酸溶液分别加水稀释,溶液中的c(H+)随溶液体积变化的曲线如图所示.据图判断下列说法正确的是( )| A. | 曲线Ⅱ表示的是盐酸的变化曲线 | |
| B. | b点溶液的导电性比c点溶液的导电性强 | |
| C. | 取等体积的a点、b点对应的溶液,消耗的NaOH的量相同 | |
| D. | b点酸的总浓度大于a点酸的总浓度 |
7.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 与Al反应能放H2的溶液中:Cu2+、NH4+、CO32-、SO42- | |
| B. | $\frac{{K}_{w}}{c(O{H}^{-})}$=10-12 mol•L-1的溶液中:Mg2+、Fe2+、NO3-、Cl- | |
| C. | 使酚酞变红的溶液中:K+、Na+、I-、AlO2- | |
| D. | 0.1 mol•L-1 FeCl3溶液中:Al3+、Ca2+、SCN-、Cl- |
4.下列制定反应的离子方程式正确的是( )
| A. | Cu与浓硝酸反应制备NO2:3Cu+8H++2NO3-═3Cu2++2NO2↑+4H2O | |
| B. | Na2S2O3溶液吸收水中多余的Cl2:4Cl2+S2O32-+5H2O=10H++2SO42-+8Cl- | |
| C. | 用惰性电极电解CuSO4溶液:2Cu2++4OH-$\frac{\underline{\;通电\;}}{\;}$2Cu↓+O2↑+2H2O | |
| D. | 向明矾溶液中滴入氢氧化钡溶液至沉淀的物质的量最大:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
11.下列有关有机化合物的说法正确的是( )
| A. | 向蛋白质溶液中滴加饱和氯化按溶液,有固体析出,蛋白质发生变性 | |
| B. | CH3CH(C2H5)CH2CH3名称为2-乙基丁烷 | |
| C. | 烷烃和苯不能发生氧化反应 | |
| D. | 甲醇与化学式为C3H8O的醇混合发生分子间脱水,可以得到6种醚 |
1.根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作与现象 | 结论 |
| A | 将Fe(NO3)2溶于稀H2SO4后,滴加KSCN溶液, 溶液变成红色 | Fe(NO3)2中一定含Fe3+ |
| B | 从煤油中取出一小块钠,用滤纸擦净表面的煤油, 放入无水乙醇中,产生气泡 | Na能置换出醇烃基中的氢 |
| C | 将某气体通入品红溶液,溶液褪色 | 气体一定是SO2 |
| D | 向NaAlO2溶液中滴入NaHCO3溶液,产生白色沉淀 | AlO2-结合H+的能力比CO32-强 |
| A. | A | B. | B | C. | C | D. | D |
8.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | $\frac{{K}_{w}}{c(O{H}^{-})}$=1×10-13mol•L-1的溶液中:Na+、K+、AlO2-、NO3- | |
| B. | 含有大量Fe3+的溶液中:NH4+、I-、Cl-、K+ | |
| C. | pH=7的溶液中:NH4+、Al3+、SO42-、NO3- | |
| D. | 0.1mol•L-1Na2SO3的溶液中:H+、Ca2+、Fe2+、Cl- |
5.下列物质的每步转化在给定条件下能一步实现且较合理的是( )
| A. | Cu2(OH)2CO3$\stackrel{H_{2}SO_{4}}{→}$CuSO4(aq)$\stackrel{Na}{→}$Cu | |
| B. | 饱和食盐水$\stackrel{NH_{3}•CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| C. | 海水$\stackrel{熟石灰}{→}$Mg(OH)2$\stackrel{△}{→}$MgO$\stackrel{电解}{→}$Mg | |
| D. | NH3$→_{催化剂,△}^{O_{2}}$N2$\stackrel{O_{2}•H_{2}O}{→}$HNO3 |
17.充分燃烧一定量的丁烷气体放出的热量为xQ kJ,完全吸收它生成的CO2生成正盐,需5mol•L-1的KOH溶液100mL,则丁烷的燃烧热为( )
| A. | 16xQ kJ•mol-1 | B. | 8xQ kJ•mol-1 | C. | 4xQ kJ•mol-1 | D. | 2xQ kJ•mol-1 |