题目内容
2010年亚运会在我国广州成功举办,整个亚运会体现了环保理念.广州亚运会火炬“潮流”采用了丙烷(C3H8)作为燃料,燃烧后的产物为水和二氧化碳.在298K时,1mol丙烷完全燃烧生成CO2和液态水放出2221.5k的热量则该反应的热化学方程式为 .
又知在298K时C3H8(g)=C3H6(g)+H2(g)△H=124.2kJ?mol-1,
H2(g)+0.5O2(g)=H2O(l)△H=-285.8kJ?mol-1,则1mol C3H6完全燃烧生成CO2和液态水时放出的热量是 kJ.
又知在298K时C3H8(g)=C3H6(g)+H2(g)△H=124.2kJ?mol-1,
H2(g)+0.5O2(g)=H2O(l)△H=-285.8kJ?mol-1,则1mol C3H6完全燃烧生成CO2和液态水时放出的热量是
考点:热化学方程式,有关反应热的计算
专题:化学反应中的能量变化
分析:依据书写热化学方程式原则分析计算,标注物质聚集状态和反应焓变写出;依据热化学方程式和盖斯定律计算所需热化学方程式;
解答:
解:在298K时,1mol丙烷完全燃烧生成CO2和液态水放出2221.5kJ的热量,则该反应的热化学方程式为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l),△H=-2221.5kJ?mol-1,
①C3H8(g)+5O2(g)=3CO2(g)+4H2O(l),△H=-2221.5kJ?mol-1,
②C3H8(g)=C3H6(g)+H2(g)△H=124.2kJ?mol-1,
③H2(g)+0.5O2(g)=H2O(l)△H=-285.8kJ?mol-1,
依据盖斯定律①-②+③得到:C3H6(g)+4.5O2(g)=3CO2(g)+3H2O(l),△H=-2059.9kJ?mol-1,1mol C3H6完全燃烧生成CO2和液态水时放出的热量2059.9kJ;
故答案为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l),△H=-2221.5kJ?mol-1;2059.9kJ;
①C3H8(g)+5O2(g)=3CO2(g)+4H2O(l),△H=-2221.5kJ?mol-1,
②C3H8(g)=C3H6(g)+H2(g)△H=124.2kJ?mol-1,
③H2(g)+0.5O2(g)=H2O(l)△H=-285.8kJ?mol-1,
依据盖斯定律①-②+③得到:C3H6(g)+4.5O2(g)=3CO2(g)+3H2O(l),△H=-2059.9kJ?mol-1,1mol C3H6完全燃烧生成CO2和液态水时放出的热量2059.9kJ;
故答案为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l),△H=-2221.5kJ?mol-1;2059.9kJ;
点评:本题考查了热化学方程式书写方法和盖斯定律的计算应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4L H2O含有的分子数为NA |
| B、4g NaOH含有的Na+离子数为0.1 NA |
| C、28g N2含有的原子数为NA |
| D、物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA |
 其分子式为
其分子式为 关于它的结构性质分析.
关于它的结构性质分析. 分子中含有的官能团名称是:
分子中含有的官能团名称是: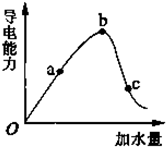 一定温度下,冰醋酸和水稀释过程中溶液的导电能力曲线如图所示,请回答:
一定温度下,冰醋酸和水稀释过程中溶液的导电能力曲线如图所示,请回答: