题目内容
用 NA表示阿伏伽德罗常数,下列关于0.2mol?L-1K2SO4溶液说法正确的是( )
| A、1L溶液中K+浓度是0.4mol?L-1 |
| B、500mL溶液中含有0.1NA个K+ |
| C、1L溶液中所含K+和SO42-总数为0.3NA |
| D、2L溶液中SO42-浓度 为0.4mol?L-1 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.1molK2SO4含有2molK+,故K+的浓度为K2SO4的2倍;
B.根据n=cV计算K+的物质的量,再根据N=nNA计算K+的数目;
C.根据n=cV计算K2SO4的物质的量,1molK2SO4含有3mol离子(2molK+,1molSO42-),再根据N=nNA计算离子的数目;
D.溶液是均一的,1molK2SO4含有1molSO42-,SO42-的浓度等于K2SO4的浓度.
B.根据n=cV计算K+的物质的量,再根据N=nNA计算K+的数目;
C.根据n=cV计算K2SO4的物质的量,1molK2SO4含有3mol离子(2molK+,1molSO42-),再根据N=nNA计算离子的数目;
D.溶液是均一的,1molK2SO4含有1molSO42-,SO42-的浓度等于K2SO4的浓度.
解答:
解:解:A.1molK2SO4含有2molK+,K+的浓度为K2SO4的2倍,K2SO4溶液为0.2mol/L,所以K+离子浓度是0.4mol/L,故A正确;
B.500mL0.2mol?L-1K2SO4溶液中,K2SO4的物质的量n=C?V=0.5L×0.2mol?L-1=0.1mol,K+的个数N=0.1×2×NA=0.2NA,故B错误;
C.1L溶液中所含K+、SO42-总数为1L×0.2mol/L×3×NAmol-1=0.6NA,故C错误;
D.溶液是均一的,每摩尔K2SO4含有1mol硫酸根,硫酸根离子的浓度等于K2SO4的浓度为0.2mol/L,故D错误.
故选A.
B.500mL0.2mol?L-1K2SO4溶液中,K2SO4的物质的量n=C?V=0.5L×0.2mol?L-1=0.1mol,K+的个数N=0.1×2×NA=0.2NA,故B错误;
C.1L溶液中所含K+、SO42-总数为1L×0.2mol/L×3×NAmol-1=0.6NA,故C错误;
D.溶液是均一的,每摩尔K2SO4含有1mol硫酸根,硫酸根离子的浓度等于K2SO4的浓度为0.2mol/L,故D错误.
故选A.
点评:本题考查阿伏加德罗常数,题目难度中等,注意注意溶液是均一的,浓度与体积无关.

练习册系列答案
相关题目
下列说法正确的是( )
| A、需要加热方能发生的反应一定是吸热反应 |
| B、放热反应在常温下一定很容易发生 |
| C、反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小 |
| D、化学反应只生成新物质,没有能量的变化 |
下列说法不正确的是( )
A、实验证实环辛四烯( )可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 )可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 |
B、已知视网醛的结构为 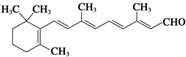 ,在它的同分异构体中属于萘( ,在它的同分异构体中属于萘( 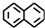 )的衍生物且能发生银镜反应的不止一种 )的衍生物且能发生银镜反应的不止一种 |
| C、三硝酸甘油酯的分子式为C3H5N3O9 |
| D、丙醇依次通过消去、加成、取代、去氢氧化、加氧氧化、还原反应可生成乳酸(2-羟基丙酸) |
下列物质完全燃烧时,生成的二氧化碳与水的物质的量相同的是( )
| A、CH4 |
| B、C6H6 |
| C、C2H5OH |
| D、C6H12O6 |
下列官能团的电子式正确的是( )
A、甲基 |
| B、羟基O:H |
C、醛基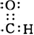 |
D、羧基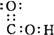 |
固体A在一定温度下分解生成气体B、C、D:2A═B↑+2C↑+3D↑,若测得生成气体的质量是同体积氢气的15倍,则固体A的摩尔质量是( )
| A、30g?mol-1 |
| B、60g?mol-1 |
| C、90g?mol-1 |
| D、120g?mol-1 |
对于下列反应类型的判断,不正确的是( )
| A、CO2+H2O=H2CO3 化合反应 |
| B、H2CO3=CO2↑+H2O 分解反应 |
| C、3CO+Fe2O3=2Fe+3CO2 置换反应 |
| D、CuO+H2=Cu+H2O氧化还原反应 |
在室温下等体积的酸和碱的溶液,混合后pH一定小于7的是( )
| A、pH=2的硝酸和pH=12的Ba(OH)2溶液 |
| B、pH=3的盐酸和pH=11的氨水 |
| C、pH=3的硫酸和pH=11的KOH |
| D、pH=4的醋酸和pH=10的KOH溶液 |