题目内容
下列官能团的电子式正确的是( )
A、甲基 |
| B、羟基O:H |
C、醛基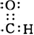 |
D、羧基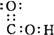 |
考点:电子式
专题:化学用语专题
分析:A.碳原子最外层有4个电子,与三个氢原子分别共用1对电子形成甲基;
B.氧原子最外层有6个电子,与1个氢原子共用1对电子形成羟基;
C.碳原子最外层有4个电子,与1个氧原子共用2对电子,与1个氢原子共用1对电子形成醛基;
D.碳原子最外层有4个电子,与1个氧原子共用2对电子形成1个C=O,与1个羟基氧原子共用1对电子形成1个C-O键,羟基中氧原子与氢原子共用1对电子对.
B.氧原子最外层有6个电子,与1个氢原子共用1对电子形成羟基;
C.碳原子最外层有4个电子,与1个氧原子共用2对电子,与1个氢原子共用1对电子形成醛基;
D.碳原子最外层有4个电子,与1个氧原子共用2对电子形成1个C=O,与1个羟基氧原子共用1对电子形成1个C-O键,羟基中氧原子与氢原子共用1对电子对.
解答:
解:A.甲基的电子式为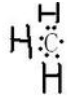 ,故A错误;
,故A错误;
B.羟基的电子式为 ,故B错误;
,故B错误;
C.醛基电子式为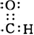 ,故C正确;
,故C正确;
D.羧基电子式为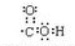 ,故D错误;
,故D错误;
故选:C.
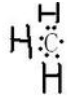 ,故A错误;
,故A错误;B.羟基的电子式为
 ,故B错误;
,故B错误;C.醛基电子式为
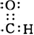 ,故C正确;
,故C正确;D.羧基电子式为
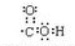 ,故D错误;
,故D错误;故选:C.
点评:本题考查了电子式的书写,明确电子式书写的原则和方法是解题关键,注意没成键的电子也必须表示出来.

练习册系列答案
相关题目
标准状况下,在体积相同的两个密闭容器中分别充满O2、O3气体,下列说法正确的是( )
| A、两种气体的质量相等 |
| B、两种气体的氧原子数相等 |
| C、两种气体的分子数相等 |
| D、两种气体的密度相等 |
在25℃下,向氨水中滴加蒸馏水,下列有关数据增大的是( )
A、
| ||
| B、c(OH-) | ||
| C、Kw | ||
| D、pH |
下列与化学反应能量变化相关的叙述正确的是( )
| A、生成物总能量一定低于反应物总能量 |
| B、放热反应的反应速率总是大于吸热反应的反应速率 |
| C、反应物和生成物所具有的总能量决定了放热还是吸热 |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下反应的△H不同 |
分析阿司匹林的结构,推知阿司匹林可以看作烃的衍生物中的( )
| A、酚类 | B、醇类 | C、醛类 | D、酯类 |
用 NA表示阿伏伽德罗常数,下列关于0.2mol?L-1K2SO4溶液说法正确的是( )
| A、1L溶液中K+浓度是0.4mol?L-1 |
| B、500mL溶液中含有0.1NA个K+ |
| C、1L溶液中所含K+和SO42-总数为0.3NA |
| D、2L溶液中SO42-浓度 为0.4mol?L-1 |
把盛有水和盐酸的两个烧杯分别放在托盘太平的左右托盘上,天平处于平衡状态,然后向右盘烧杯里加入镁,向左盘烧杯里加入与镁等质量的金属钠,当金属完全反应后,天平的指针( )
| A、向左偏转 | B、向右偏转 |
| C、仍处于平衡状态 | D、不能确定 |
下列说法正确的是( )
| A、凡是中心原子采取sp3杂化的分子,其立体构形都是正四面体 |
| B、杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 |
| C、CH4分子中的sp3杂化轨道是由4个H的1s轨道和C原子的2p轨道混合起来而形成的 |
| D、凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键 |
 化学是一门以实验为基础的科学,熟练使用中学化学实验中的常见仪器,熟悉常见实验用品是正确进行实验的基础.试回答以下问题:
化学是一门以实验为基础的科学,熟练使用中学化学实验中的常见仪器,熟悉常见实验用品是正确进行实验的基础.试回答以下问题: