题目内容
密闭容器中进行的反应2SO2+O2?2SO3温度保持不变,下列说法中正确的是( )
| A、增加SO2的浓度,正反应速率先增大,后逐渐减小最后保持不变 |
| B、增加O2的浓度,正反应速率逐渐增大 |
| C、增加SO2的浓度,平衡常数增大 |
| D、若平衡时SO2的浓度比原来大,则平衡常数增大 |
考点:化学反应速率的影响因素,化学平衡的影响因素
专题:
分析:增大反应物浓度,单位体积活化分子数目增多,正反应速率增大,反应向正向移动,达到平衡时,正逆反应速率相等,平衡常数只与温度有关,温度不变,平衡常数不变,以此解答该题.
解答:
解:A.增加SO2的浓度,单位体积活化分子数目增多,正反应速率先增大,反应向正向移动,随着反应的进行,反应物的浓度逐渐减小,则正反应速率后逐渐减小最后保持不变而达到平衡状态,故A正确;
B.增加O2的浓度,正反应速率瞬间增大,后逐渐减小,故B错误;
C.增加SO2的浓度,如温度不变,则反应速率不变,故C错误;
D.平衡常数只与温度有关,温度不变,平衡常数不变,故D错误.
故选A.
B.增加O2的浓度,正反应速率瞬间增大,后逐渐减小,故B错误;
C.增加SO2的浓度,如温度不变,则反应速率不变,故C错误;
D.平衡常数只与温度有关,温度不变,平衡常数不变,故D错误.
故选A.
点评:本题考查较为综合,涉及化学平衡状态的判断、平衡移动原理等,为高频考点,侧重于学生的分析能力的考查,难度不大,要注意把握平衡状态的特征.

练习册系列答案
相关题目
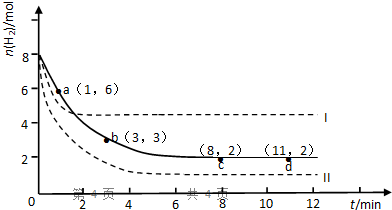
一定条件下存在反应:2SO2(g)+O2(g)═2SO3(g),△H<0.现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如图所示投料,并在400℃条件下开始反应.达到平衡时,下列说法正确的是( )


| A、容器Ⅰ、Ⅲ中平衡常数相同 |
| B、容器Ⅱ、Ⅲ中正反应速率相同 |
| C、SO3的体积分数:Ⅱ<Ⅲ |
| D、容器Ⅰ中SO2的转化率与容器Ⅱ中SO3的转化率之和小于1 |
以下实验操作正确的是( )
| A、用量筒量取5.0 mL浓硫酸并直接在量筒中稀释 |
| B、用嘴吹灭燃着的酒精灯火焰 |
| C、称量NaOH固体时,将药品直接放在托盘上 |
| D、给烧瓶里的液体加热时,垫上石棉网 |