题目内容
二氧化钛(TiO2)是一种用途广泛的化工原料,用四氯化钛(TiCl4)与某常见物质X反应可制得二氧化钛,反应的化学方程式为:TiCl4+□X=TiO2+4HCl,关于物质X下列说法正确的是( )
| A、该物质由碳、氢、氧三种元素组成 |
| B、该物质的化学式为H2O2 |
| C、该物质中氢、氧元素的质量比1:8 |
| D、该物质中氢元素的质量分数为5% |
考点:质量守恒定律
专题:计算题
分析:根据质量守恒定律的元素守恒、原子种类和个数不变,结合反应的化学方程式为:TiCl4+□X═TiO2+4HCl,推测物质X的有关信息.
解答:
解:根据质量守恒定律的元素守恒、原子种类和个数不变,结合反应的化学方程式为:TiCl4+□X═TiO2+4HCl,
推测X的化学式为H2O,则:
A.该物质由氢、氧两种元素组成,故A错误;
B.该物质的化学式为H2O,故B错误;
C.该物质的化学式为H2O,故该物质中氢、氧元素的质量比为1×2::1=1:8,故C正确;
D.该物质的化学式为H2O,故该物质中氢元素的质量分数为
×100%=11.1%,故D错误;
故选:C.
推测X的化学式为H2O,则:
A.该物质由氢、氧两种元素组成,故A错误;
B.该物质的化学式为H2O,故B错误;
C.该物质的化学式为H2O,故该物质中氢、氧元素的质量比为1×2::1=1:8,故C正确;
D.该物质的化学式为H2O,故该物质中氢元素的质量分数为
| 1×2 |
| 1×2+16 |
故选:C.
点评:本题考查运用质量守恒定律推断物质的化学式,难度不大.要注意结合物质的性质,灵活应用.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
下列离子在溶液中能大量共存的是( )
| A、Na+、CO32-、SO42-、H+ |
| B、K+、OH-、H+、Cl- |
| C、Mg2+、H+、NO3-、SO42- |
| D、Fe3+、K+、OH-、NO3- |
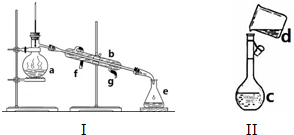
下图所示四种化学实验操作的名称按①②③④顺序排列分别为( )


| A、过滤、蒸发、蒸馏、萃取(或分液或萃取分液) |
| B、过滤、蒸馏、蒸发、萃取 |
| C、蒸发、蒸馏、过滤、萃取 |
| D、萃取、蒸馏、蒸发、过滤 |
蛋白质是人体必需的重要营养成分之一.下列食物中,富含蛋白质的是( )
| A、豆油 | B、馒头 | C、西红柿 | D、豆腐 |
下表中元素均为中学化学中常见短周期元素,根据表中信息,下列说法不正确的是( )
| 元素代号 | X | Y | Z | W | N |
| 原子半径/nm | 0.186 | 0.074 | 0.102 | 0.099 | 0.160 |
| 主要化合价 | +1 | -2 | -2、+6 | +7、-1 | +2 |
| A、X的最高价氧化物对应水化物的碱性比N的强 |
| B、由X、Y、Z三种元素只能组成一种含有离子键和共价键的化合物 |
| C、化台物X2Z的晶体类型与NW2的晶体类型相同 |
| D、由X和Y形成的一种淡黄色固体化合物中阴、阳离子个数比为1:2 |
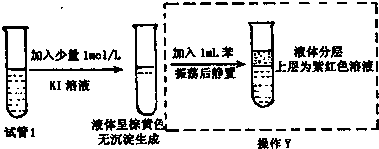

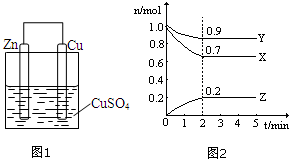 (1)设计的原电池如图1所示,回答下列问题:
(1)设计的原电池如图1所示,回答下列问题: